百日咳
百日咳に関する近年のトピックス
百日咳は現行の予防接種で抑制が十分できておらず、局地的な流行が断続的に起きています。重症化のリスクのある新生児での発生報告も途絶えていません。百日咳の流行状況や対策について、まずはポイントをまとめてみました。気になった方は、ぜひ次項からの本文をお読みください。
・百日咳は予防接種の効果が長期間持続しないため、学童や成人での発症が増加している。重症になりやすい乳児への感染も現行の予防接種体制では十分防ぐことができておらず、死亡例も報告されている。
・定期接種のスケジュールに加え、日本小児科学会は5-6歳、11-12歳での任意接種による追加を推奨している。しかし、海外で同様の対策をしている地域の報告を見ると、百日咳ワクチンの追加接種対象を広げるだけでは流行を抑えきれず限界がある。早期乳児への感染対策としては、妊娠後期の妊婦への予防接種が最も効果が高いというデータが蓄積され、海外ではこれを導入する国が増えている。
・成人例を含めた発生動向の正確な調査のため、2018年に感染症法で5類小児科定点把握疾患から5類全数把握疾患に変更され、届出基準も改定された。
・2016年にLAMP法、IgA抗体測定、IgM抗体測定といった検査項目が新しく保険収載された。特にLAMP法は、感度の限界はあるものの従来困難であった早期診断を可能にした。
微生物
百日咳菌(Bordetella pertussis)は、主に呼吸器感染症を起こす小型のグラム陰性桿菌である。ごくまれに菌血症を起こすこともある。類縁の細菌として、パラ百日咳菌(Bordetella parapertussis)やBordetella holmesiiがあるが、百日咳菌に比べると百日咳毒素産生がなく、より軽症である場合が多い[1]。
歴史と疫学
百日咳は1940年代ごろまでは多くの感染者、死亡者を出す疾患であったが、1950年に予防接種が導入され、1968年には全細胞型3種混合ワクチン(破傷風、ジフテリア、百日咳)の定期接種が開始されて患者数は激減した。しかし、1975年にワクチン接種後の死亡事例があり、百日咳ワクチンによる脳症が原因と考えられたため、一時中止された。数か月後に接種時期を引き上げて再開されたが接種率は低く、1979年には百日咳の報告が年間約13,000例、死亡数が約20例以上と増加してしまった。1981年には副作用の多かった全細胞ワクチン(whole cell vaccination)から日本で研究・開発された無細胞ワクチン(acellular vaccination)に変更され、3種混合ワクチンの接種率は改善し、再び百日咳の発症は減少へと向かった[2]。
しかし、2000年以降になってから、百日咳の局地的な流行が散発するようになった。百日咳の予防接種は4~12年で効果が減弱するため、思春期や成人での発症が相対的に増加した影響と考えらえる。最大のアウトブレイクとしては、大学で学生や職員約300人に感染が拡大した事例がある[3]。日本のみならず世界的にも発症年齢が上昇する傾向が見られた。
百日咳の増加に伴い、リスクの高い乳児の重症例が報告されている。東京都立小児総合医療センターの2010年3月~2018年11月の百日咳のデータ集計によると、百日咳患者131例中73例が入院症例で、重症が43例(年齢中央値3か月)、死亡が3例であった[4]。
日本でのサーベイランスは、以前は5類小児科定点把握疾患で成人の報告が少なく、届出基準が臨床症状のみでの判断であったことから、百日咳の正確な発生動向を把握することが困難であった。2018年に百日咳は5類全数把握疾患となり、LAMP法など新たな検査が開発されたことを受けて、届出基準も「臨床症状と検査陽性」または「臨床症状と百日咳患者との接触歴」を満たすことに変更され、より広くかつ正確な状況把握ができるようになった。
表1 感染症法における百日咳の新旧届出基準(抜粋)| 以前の百日咳届出基準 (5類小児科定点把握疾患) | 2018年改定後の百日咳届出基準 (5類全数把握疾患) |
| 届出のために必要な臨床症状(ア及びイを満たすもの) ア 2週間以上持続する咳嗽 イ 以下のいずれかの要件のうち少なくとも1つを満たすもの (ア)スタッカート及びウープを伴う咳嗽発作 (イ)新生児や乳児で、他に明らかな原因がない咳嗽後の嘔吐又は無呼吸発作 | ・百日咳を疑う臨床症状:スタッカートやウープを伴う咳嗽発作、嘔吐や無呼吸発作、非特異的な持続する咳嗽など ・百日咳の検査:培養、遺伝子検査、抗体検査 ・百日咳患者と接触がある場合は、臨床症状のみで検査なしでも届出可 |
5類全数把握疾患となってからの2018年1月1日~2018年9月30日までの百日咳のデータの集計が、国立感染症研究所から発表されている[5]。この期間で報告された症例の中で届出基準を満たしたものは6,443例であった。そのうち、5歳から15歳未満までの学童期の小児が65%で、6~9歳が特に多かった。重症化のリスクのある6か月未満児は5%、30~50代の成人は14%であった。乳児期の4回の予防接種を完遂できている症例が多く、特に5~15歳未満の約8割で予防接種が行われていた。また、6か月未満の患児では家族(同胞、両親)からの感染が多かった。この結果からは、特に学童期での追加接種が、社会全体への高い予防効果をもたらすと考えられる。
検査法は、小児ではLAMP法が多く、15歳以上では単一血清抗体価での診断が50%以上であった。成人でのLAMP法の実施が十分に普及していない懸念がある。
また、5類全数把握疾患となった直後でもあり、医師が百日咳と診断しても届出義務があると知らずに報告していないケースもあると予想される。
日本と海外での予防接種スケジュールの違い
日本での現行の予防接種は4種混合ワクチン(ジフテリア、百日咳、破傷風、ポリオ)が定期接種となっており、生後3、4、5か月および12か月の4回行われる。日本小児科学会は、2018年8月に予防接種スケジュールの推奨を改定し、5~6歳、11~12歳で3種混合ワクチンの接種を加えることを推奨しているが、この時期の接種は任意接種で全額費用負担が必要となる[6]。
海外では接種開始が生後2か月から始まることが多く、また4~6歳の就学前の3種混合ワクチンも広く普及している。一部の国では思春期~青年期に成人用3種混合ワクチン(Tdap)を接種している[7]。
しかし、海外の発生動向を見ると、追加接種回数を増やすだけでは百日咳の流行を抑えるには不十分であることが分かってきた。そこで、現在早期乳児への感染対策として注目されているのが妊娠後期の妊婦への予防接種(妊娠ごとに毎回)である。アメリカやイギリス、ニュージーランドなどで導入され、高い効果を示している[8]。ニュージーランドの調査では、百日咳の流行があっても妊娠後期にワクチン接種を行った母親から産まれた新生児では百日咳の発症は1例も見られなかった[9]。
ただ、諸外国で妊娠後期に接種されている成人用のTdapは日本では未承認で、輸入ワクチンとしてのみ接種可能である。日本で発売されている3種混合ワクチン「トリビック®」も成人に接種可能だが、添付文書には「妊娠中の接種に関する安全性は確立していないので、妊婦又は妊娠している可能性のある婦人には予防接種上の有益性が危険性を上回ると判断される場合にのみ接種すること」と記載されていて、現時点では妊婦への予防接種をルーチンで実施することは難しい。今後、予防接種スケジュールを見直す上で、妊娠後期での追加接種は最も検討すべき課題と考える。
感染経路
百日咳菌は、上気道分泌物の飛沫や直接接触により上気道に感染し、気管支の粘膜上皮や繊毛間で増殖する。
症 状
百日咳は曝露から約1週間(6~20日)で発症する。(1)カタル期、(2)痙咳期、(3)回復期の順に進行する(図1)[10]。
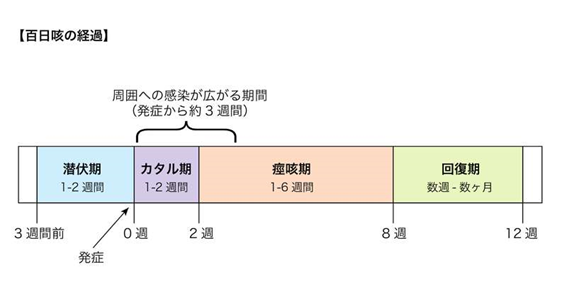 図1 百日咳の経過
図1 百日咳の経過(https://medley.life/news/5c85e262b78d102e9bef1524/)
・参考文献:CDC: Pertussis (Whooping Cough), Clinical Features. last reviewed:August 7, 2017. (https://www.cdc.gov/pertussis/clinical/features.html)
1.経 過
1)カタル期
初期は鼻汁や咳で始まり、一見通常の風邪症候群と区別が付かない。しかし、排菌量はこの時期が最も多く「診断しにくく拡散しやすい」というジレンマを抱える。1~2週続いた後に痙咳期に移行する。
2)痙咳期
この時期になると、連続性の咳(paroxysmal cough, staccato)、吸気性笛声(whooping cough)、咳込み後の嘔吐といった典型的な百日咳の症状が出現する。インターネットの動画サイトで、いくつか実際の所見を視聴することができる。乳児や予防接種歴のある患者では、典型的な症状が出にくい。2017年のシステマティック・レビューでは、吸気性笛声は特異度が高く、発作性咳嗽は感度が高いという結果であったが、いずれも陽性尤度比(LR+)、陰性尤度比(LR−)は十分な値ではなかった(表2)[11]。当然ではあるが、やはり単一の臨床症状だけでの診断は難しい。医師が総合的な判断で臨床的に百日咳を疑う場合、感度はさほど高くはないが、特異度やLR+は比較的高いという興味深い結果もあった。
小児では、咳き込み後の嘔吐の感度は成人よりも高く、特異度は低い。百日咳に限らず小児は成人よりも咳嗽に伴う嘔吐を起こしやすいことからも、小児ではあまり鑑別には有用ではないのだろう。
痙咳期は1~6週と個人差がある。痙咳期の後半になると、細菌は排除され、咳症状があっても周囲への感染性は乏しくなる。
表2 百日咳の症状| 感度 | 特異度 | LR+ | LR− | |
| 吸気性笛声 | ||||
| 小児 | 41%(24-61) | 84%(52-96) | 2.9(1.2-7.3) | 0.72(0.60-0.84) |
| 成人 | 21%(16-28) | 82%(70-90) | 1.2(0.81-1.8) | 0.97(0.81-1.8) |
| 咳き込み後の嘔吐 | ||||
| 小児 | 56%(39-72) | 66%(52-78) | 1.7(1.3-2.2) | 0.67(0.49-0.84) |
| 成人 | 34%(26-43) | 80%(74-84) | 1.7(1.3-2.3) | 0.83(0.73-0.93) |
| 発作性咳嗽 | ||||
| 小児 | 72%(60-81) | 47%(32-62) | 1.4(1.2-1.7) | 0.61(0.52-0.72) |
| 成人 | 88%(80-92) | 26%(12-47) | 1.2(1.04-1.6) | 0.50(0.33-0.75) |
| 総合的な印象 | 47%(36-59) | 85%(71-93) | 3.3(1.9-5.5) | 0.63(0.56-0.70) |
| 発熱 | 13%(5-29) | 82%(71-90) | 0.76(0.45-1.2) | 1.0(0.95-1.1) |
3)回復期
発作的な連続性の咳は治るが、軽度の咳が持続する。また、この時期に新たに別の呼吸器感染症に罹患すると発作性咳嗽が再燃しやすい。症状改善まで数週~数か月かかる。
2.乳児での合併症
乳児、特に生後3か月以内は重症化のリスクが高い。この時期の小児では典型的な咳嗽所見がないことが多く、無呼吸発作が主体となることもあり注意が必要である。入院が必要となる乳児では、無呼吸 61%、肺炎 23%、痙攣 1%、脳症 0.1%といった合併症を認める。1%で死亡に至る[10]。
3.予防接種歴がある場合の百日咳
予防接種歴がある場合には典型的な強い咳嗽発作は出にくく、非特異的な咳嗽が長く続く以外に症状に乏しいことが多い。前述の2007年の日本でのアウトブレイクでは、予防接種歴がある場合の発作性咳嗽の頻度は約60%であった。
鑑別診断
急性咳嗽(3週以内)や遷延性咳嗽(3~8週)をきたす疾患が鑑別となり、マイコプラズマなど非定型肺炎や結核、感染後咳嗽、咳喘息など多岐にわたる。発熱が乏しいことや乾性咳嗽であること、肺炎はまれであること、咳が発症時から増悪傾向であること(特に発作性・連続性)が、百日咳を疑うきっかけとなる。症状や経過に合わせて適切な検査を進める。
検 査
1.培養検査
培養検査は菌の証明を確定することができるだけでなく、追加で薬剤感受性試験や遺伝子解析を行うことができるため、臨床的にも公衆衛生的にも重要な検査である。しかし、実際に培養で菌を検出することは難しい場合が多い。
まず検体は、鼻咽頭スワブや、鼻を生理食塩水で洗浄し、吸引したものから、鼻咽頭粘液を採取する。スワブの場合、通常の綿棒は不飽和脂肪酸を含み百日咳菌の発育を抑制するため、レーヨン性の専用の綿棒(コレクトスワブRアルミ軸 ® 、栄研化学)を用いる。また、百日咳の培養にはBG(Bordet-Gengou)培地やRegan-Lowe charcoal培地、CSM(cyclodextrin solid medium)培地などの選択培地が必要となるため、微生物検査室に百日咳を疑っていることを伝える必要がある。
培養の感度は低く、比較的陽性になりやすい乳児でも60%以下で、報告によっては10%前後である[12、13]。特に発症2週以上を過ぎると検出できることはまれである。予防接種歴がある場合や、抗菌薬投与によっても感度は低下する。また、陽性になるまで5~7日間かかる。百日咳菌の肺炎発症時などで、まれに喀痰のグラム染色や培養で検出できることがある(図2)。
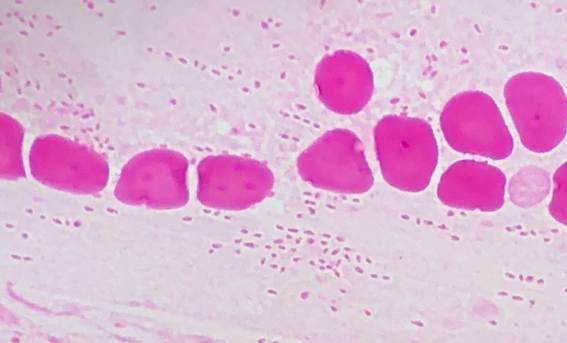
(兵庫県立尼崎総合医療センターER総合診療科/感染症内科 松尾裕央先生からご提供)
2.遺伝子検査
遺伝子検査は、従来困難であった百日咳の早期診断を可能とした画期的な検査である。培養よりも感度が高く、抗菌薬の影響を受けにくい。リアルタイムPCRでは感度は約4割前後と限界はある。特異度は報告により様々で、偽陽性のリスクもある[13]。
発症3週以内での検査が望ましいが、死菌でも反応するため発症から4週までであれば陽性になることもある。2016年に保険収載されたLAMP法は、従来のリアルタイムPCRに比べ前処理が簡易で迅速に結果が判明し、感度・特異度もほぼ同等であることから日常臨床で利用しやすく、最も有用な検査である[14]。
3.百日咳抗体
1)PT(pertussis toxin) IgG抗体
百日咳毒素に対する抗体で、感染2週以降で陽性化する。百日咳ワクチン接種や母体からの移行抗体による偽陽性があり、判定は悩ましいことがある。また、単回の検査ではなくペア血清で判断が必要なこともある。ペア血清の理想的な検査のタイミングとしては、発症2週以内に初回採取し、その4週後に2回目の検査を行う。初回検査が遅れた場合は、すでに抗体価がピークとなっていることもある。
日本小児呼吸器感染症診療ガイドライン[15]では、下記のような判定基準を推奨している。
・初回検査で陰性の場合は、発症4週以内であればペア血清を行い、抗体価が10EU/mL以上に陽転化すれば百日咳の可能性が高く、陰性のままであれば百日咳ではないと判断する。発症4週以上で陰性の場合は、百日咳の可能性は低い。
・初回検査で弱~中等度陽性(10~99EU/mL)の場合は、ワクチン接種歴がなければ百日咳の可能性が高いと判断できるが、ワクチン接種歴がある場合や不明な場合はペア血清で確認を行い、2倍以上に上昇していれば百日咳と確定、上昇がなければ百日咳ではないと判定する(ペア血清の判定基準は定まったものはなく、日本では2倍以上を基準とすることが多いが、典型的には4倍以上となる)。
・抗体価が100EU/mL以上の場合は、単回でも百日咳の可能性が高い。ただし、乳児期早期の予防接種直後でも100EU/mL以上となることがある。
このように早期診断には不向きで、結果の解釈が悩ましいことも多いため、日常臨床での実用性はやや低い。
2)FHA(filamentous hemagglutinin) IgG抗体
日本ではPT IgG抗体測定と同時に測定しているが、他国では使用されていない。百日咳ワクチン接種や百日咳菌以外のBordetella属やHaemophilus influenzae、Mycoplasma pneumoniae、Chlamydophila pneumoniaeといった菌でも陽性になる。
3)IgM抗体、IgA抗体
百日咳菌に対するIgM抗体、IgA抗体が2016年に保険収載となった。いずれもワクチンの影響を受けないため単回で診断可能である。IgM抗体は発症15日、IgA抗体は発症21日がピークで、IgA抗体がIgM抗体よりも陽性期間は長い[15]。結果は、陰性、判定保留、陽性のいずれかで報告される。判定保留の際は、発症後早期であれば2-3週後に再検査、あるいはLAMP法で検査を行う。
4.その他
・白血球数
白血球数は正常~軽度上昇を認め、分画ではリンパ球が上昇していることが多い[16]。乳児では白血球数30,000/μL以上と重症化に相関を認めた[17]。
治 療
カタル期に抗菌薬を開始すると咳症状は軽減するが、百日咳患者との接触や周囲での流行などの情報がないと治療開始の判断は難しい。家族に乳児がいるなどのリスクがなければ、抗菌薬適正使用の観点からも安易な処方は慎みたい。痙咳期での抗菌薬は本人の症状の改善にはつながらないが、周囲への感染拡大を抑制する。抗菌薬を開始して約5日で菌は陰性化する。回復期は抗菌薬の投与は不要である。
抗菌薬第1選択はアジスロマイシンまたはクラリスロマイシンで、第2選択はST合剤である[18]。生後1か月未満の乳児ではアジスロマイシンを使用する。エリスロマイシンは乳児肥厚性幽門狭窄症のリスクがあるが、同じマクロライド系のアジスロマイシンで乳児肥厚性幽門狭窄症が増加するかどうか厳密には結論は出ていない。ただ、エリスロマイシンほど関連性はないと考えられており、必要な場合にはためらわずに使用する[19]。ST合剤は、新生児や低出生体重児で黄疸のリスクがあるため、生後2か月以降で使用する(表3)[20]。
| 年齢 | アジスロマイシン*1 | クラリスロマイシン*2 | ST合剤*4 |
| 1か月未満 | 10mg/kg/day・5日間 | 推奨しない | 2か月以内は禁忌 |
| 1~5か月 | 10mg/kg/day・5日間 | 15mg/kg/day・7日間(最大1g) | 2か月以上で使用 TMP 8mg/kg/day, SMX 40mg/kg/day (最大TMP 320mg/day, SMX 1600mg/day)・14日間 |
| 6か月以上の小児 | 初日:10mg/kg (最大500mg) 第2~5日:5mg/kg/day (最大250mg) | ||
| 成人 | 初日:500mg/day 第2~5日:250mg/day | 1g/day・7日間*3 | TMP320mg/day, SMX1600mg/day・14日間 |
*2 クラリスロマイシンは、1日量を2分割して投与する。
*3 クラリスロマイシンは、米国では1錠当たり250mgの製剤で1gの2分割投与が容易だが、日本では1錠当たり200mgの製剤で、添付文書では一般感染症に対して400mg/日が上限となるため、保険診療上は1g/日投与は行いにくい。
*4 ST合剤は、1日量を2分割して投与する。日本では1錠当たりトリメトプリム80mg、スルファメトキサゾール400mgのsingle-strength錠が使用されており、成人で1日4錠分2での投与を行う。
(文献20より引用改変)
予防内服
アメリカ疾病管理予防センター(Centers for Disease Control and Prevention: CDC)では、百日咳に曝露した際の予防内服(postexposure antimicrobial prophylaxis: PEP)を患者と同居している家族、高リスク群(乳児、妊娠後期、免疫不全、中等度から重度の喘息)、高リスク群と密接に接触する人に推奨している[21]。実施する場合は、曝露後21日以内に治療と同じレジメンで行う。
まとめ
百日咳は散発的な流行を繰り返し、現行の予防接種では乳児の重症百日咳の予防が十分できていない。今後、学童期や思春期だけでなく、妊娠後期での予防接種追加を含めた予防接種スケジュールの見直しをはじめとする対策が必要である。
現時点でできることとして、慢性咳嗽や咳の程度が強いときには百日咳を鑑別に挙げることを忘れないようにしたい。特に乳児への感染を防ぐためには、病歴聴取の際に乳児と同居しているか、乳児と身近に接する職業かをルーチンで確認し、乳児への感染源となりやすい同居家族、保育士、教師、医療従事者などでは百日咳の検査や治療の閾値を下げることが望ましい。
また、百日咳には上述してきたような多くの課題があること、5類全数把握疾患となり届出義務があることを特に小児科以外の医師にも周知し、百日咳が小児だけの問題ではないという認識を様々な診療科の医師が共有することも重要である。
【References】
1)Mattoo S, Cherry JD: Molecular pathogenesis, epidemiology, and clinical manifestations of respiratory infections due to Bordetella pertussis and other Bordetella subspecies. Clin Microbiol Rev. 2005 Apr; 18(2): 326-82.
2)国立感染症研究所: 百日せきワクチン ファクトシート, 2017.
https://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000184910.pdf
3)Kamano H, Mori T, Maeta H, et al: Analysis of Bordetella pertussis agglutinin titers during an outbreak of pertussis at a university in Japan. Jpn J Infect Dis. 2010 Mar; 63(2): 108-12.
4)米田立, 福岡かほる, 堀越裕歩・他: 小児病院での重症の百日咳菌感染症. IASR. 40: 5-6, 2019.
https://www.niid.go.jp/niid/ja/allarticles/surveillance/2438-iasr/related-articles/related-articles-467/8548-467r03.html
5)国立感染症研究所感染症疫学センター・同細菌第二部: 新しい百日咳サーベイランスによる国内の百日咳の疫学(2018年疫学週第1週~39週).
https://www.niid.go.jp/niid/ja/pertussis-m/pertussis-idwrs/8043-pertussis-180517.html
6)日本小児科学会: 日本小児科学会が推奨する予防接種スケジュールの変更点, 2018.
http://www.jpeds.or.jp/uploads/files/vaccine_schedule.pdf
7)神谷元: 海外の百日せき含有ワクチンの予防接種スケジュールと百日咳対策. IASR. 38: 37-38, 2017.
https://www.niid.go.jp/niid/ja/allarticles/surveillance/2404-iasr/related-articles/related-articles-444/7084-444r09.html
8)手塚宜行, 小熊博子, 松尾嘉人・他: 侮れない百日咳に立ち向かうために. 小児感染免疫. 28(4): 325-33, 2017.
9)Walls T, Graham P, Petousis-Harris H, et al: Infant outcomes after exposure to Tdap vaccine in pregnancy: an observational study. BMJ Open. 2016 Jan 6; 6(1): e009536.
10)CDC: Pertussis(Whooping Cough), Clinical Features.
https://www.cdc.gov/pertussis/clinical/features.html
11)Ebell MH, Marchello C, Callahan M: Clinical Diagnosis of Bordetella Pertussis Infection: A Systematic Review. J Am Board Fam Med. 2017 May-Jun; 30(3): 308-19.
12)Templeton KE, Scheltinga SA, van der Zee A, et al: Evaluation of real-time PCR for detection of and discrimination between Bordetella pertussis, Bordetella parapertussis, and Bordetella holmesii for clinical diagnosis. J Clin Microbiol. 2003 Sep; 41(9): 4121-6.
13)Bamberger E, Lahat N, Gershtein V, et al: Diagnosing pertussis: the role of polymerase chain reaction. Isr Med Assoc J. 2005 Jun; 7(6): 351-4.
14)Torkaman MR, Kamachi K, Nikbin VS, et al: Comparison of loop-mediated isothermal amplification and real-time PCR for detecting Bordetella pertussis. J Med Microbiol. 2015 Apr; 64(Pt 4): 463-5.
15)小児呼吸器感染症診療ガイドライン作成委員会: 小児呼吸器感染症診療ガイドライン2017, 協和企画, 2017.
16)Heininger U, Klich K, Stehr K, et al: Clinical findings in Bordetella pertussis infections: results of a prospective multicenter surveillance study. Pediatrics. 1997 Dec; 100(6): E10.
17)Murray EL, Nieves D, Bradley JS, et al: Characteristics of Severe Bordetella pertussis Infection Among Infants ≤90 Days of Age Admitted to Pediatric Intensive Care Units – Southern California, September 2009-June 2011. J Pediatric Infect Dis Soc. 2013 Mar; 2(1): 1-6.
18)CDC: Pertussis(Whooping Cough), Treatment.
https://www.cdc.gov/pertussis/clinical/treatment.html
19)Smith C, Egunsola O, Choonara I, et al: Use and safety of azithromycin in neonates: a systematic review. BMJ Open. 2015 Dec 9; 5(12): e008194.
20)Tiwari T, Murphy TV, Moran J; National Immunization Program, CDC: Recommended antimicrobial agents for the treatment and postexposure prophylaxis of pertussis: 2005 CDC Guidelines. MMWR Recomm Rep. 2005 Dec 9; 54(RR-14): 1-16.
21)CDC: Pertussis(Whooping Cough), Postexposure Antimicrobial Prophylaxis.
https://www.cdc.gov/pertussis/outbreaks/pep.html