WHOが推奨する 新しい抗菌薬適正使用の基準 ――AWaRe分類
抗菌薬選択の適正性を判断することの難しさ
2016年に日本における薬剤耐性(AMR)対策アクションプランが策定されたことで、医療者の薬剤耐性に対する意識はだいぶ変わってきたように思う。一般市民への啓発はまだまだこれからの面もあるが、少しずつ浸透してきていることも実感される。とある感染症医は、美容室に髪を切りに行ったとき、たまたま隣で髪を切っていた客が美容師と薬剤耐性の話をしているのを聞き、感動のあまり涙を流したという(目に髪の毛が入ったと勘違いされたらしいが)。
さて、その甲斐もあり、2016年まで横ばいであった日本の抗菌薬使用量(販売量ベース)は2017年、2018年と継続的に減少し、ついに2013年比で10.7%の減少に至った(図1)[1]。もちろん、これはこれでAMRを生み出す選択圧が減少しているという意味で大切なことなのだが、抗菌薬使用量そのものが減少することよりも、「抗菌薬が適切に選択される」ことがより大切であろう。抗菌薬が適切に選択された結果として、抗菌薬使用量が減少することがわれわれの目標である。
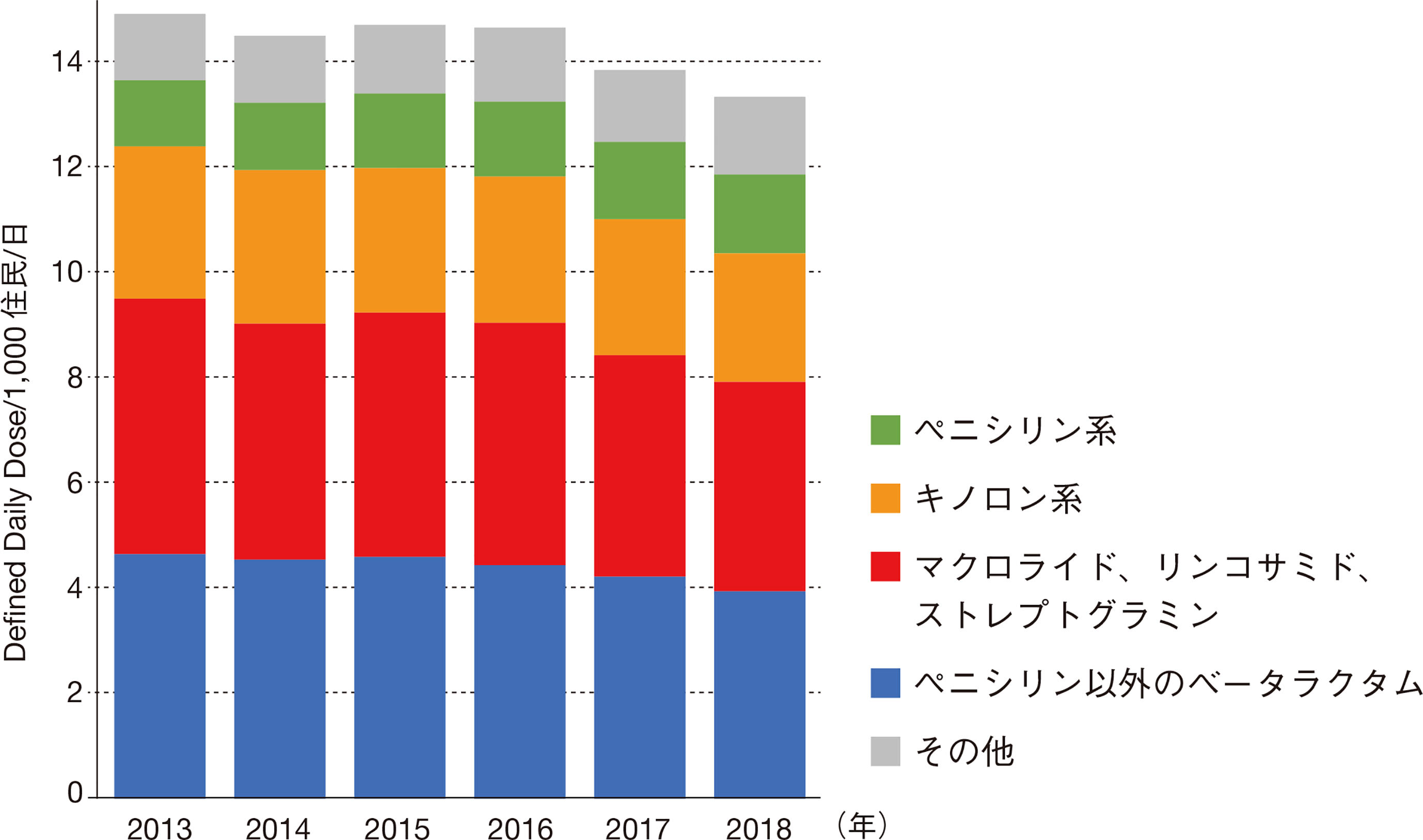
(文献1より引用改変)
しかしながら、抗菌薬使用量のデータから抗菌薬選択の適正性を判断するのは結構難しい。なぜなら、たとえ同じ抗菌薬であっても、抗菌薬選択の適正性は使用された疾患によって異なるからである。例えば、アモキシシリン・クラブラン酸が難治性中耳炎に使用された場合は適切と言えるが、溶連菌性咽頭炎に使用された場合は不適切である。つまり、抗菌薬選択の適正性をデータで観察するためには、疾患の側から処方をみる必要がある。
そのためには、保険のデータベース(ナショナル・データベース[2]など)を使って病名と処方を突き合わせて評価する必要があるのだが、この場合、登録されている病名が本当にその病気にかかって付けられているのか、それとも保険請求のために付けられているのかが分からないという問題が生じてしまう(例えば、抗菌薬を使用した急性上気道炎の患者について、査定されないために「肺炎」と病名を付けておくなど)。このため、どうしても調査に限界が生じてしまうのである。抗菌薬適正使用における先進国であるスウェーデンでは、すでに急性中耳炎や尿路感染症にどの抗菌薬が使用されているかをグループ間でモニタリングするシステムがあるが[3、4]、このようなモニタリングシステムは日本を含め、多くの国ではまだ実現が難しい状況である。
抗菌薬適正使用を評価するAWaRe分類
そうした中、2019年6月、WHOが抗菌薬使用量から抗菌薬適正使用を判断するための新たな指標を打ち出した。それがAWaRe分類を利用した指標である。AWaRe分類のもととなったのは、2017年3月に公開されたWHO文書「WHO Model Lists of Essential Medicines 第20版」である[5]。このリストは、現在および未来にわたって国の基本的な医療需要を満たすために、最低限必要な薬剤を収載したリストであり、第20版から抗菌薬が“Access”“Watch”“Reserve”の3つのカテゴリーに分類されることになった。
“Access”に分類される抗菌薬は、一般的な感染症(21の感染症について検討されている)の第一選択薬または第二選択薬として用いられる耐性化の懸念の少ない抗菌薬で、すべての国が、高品質かつ手頃な価格で、広く利用できるようにすべきものと定義されている。“Watch”に分類される抗菌薬は、耐性化が懸念されるため、限られた疾患や適応にのみ使用すべき抗菌薬と定義されている。そして、“Reserve”に分類される抗菌薬は、AMRのために他の手段が使用できなくなったときにのみ使用される、最後の手段(last resort)として取り扱うべき抗菌薬と定義されている。もちろん、AMRを拡散させる懸念があり、同時に一般的な感染症の第一選択薬または第二選択薬として用いられる抗菌薬もあるため、“Access”かつ“Watch”である抗菌薬も存在する。それぞれのカテゴリーに分類されている抗菌薬を図2[6]にまとめる。
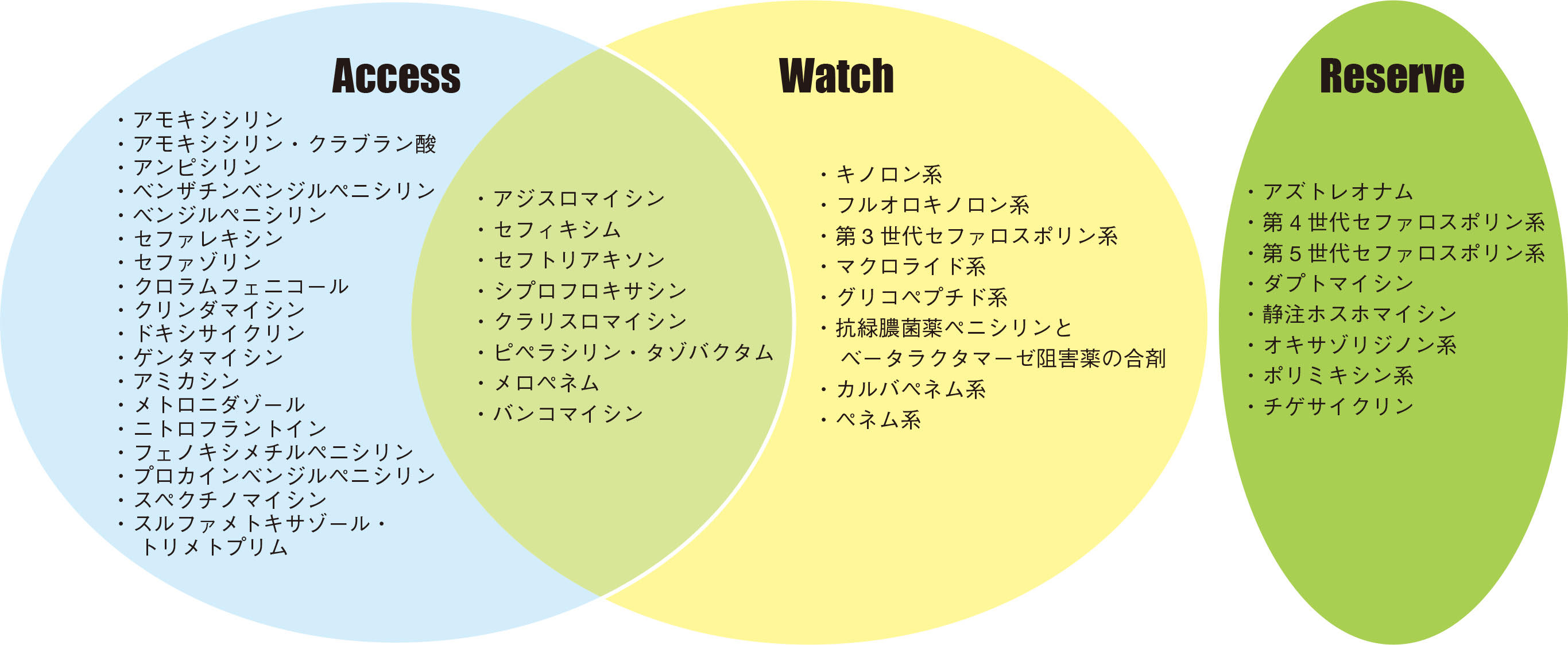
図2 Access/Watch/Reserveそれぞれに分類される抗菌薬
(文献6より引用改変)
この分類を、抗菌薬適正使用の指標に利用しようというのがWHOの狙いである。すべての抗菌薬の中で“Access”に分類される抗菌薬をなるべく増やし、“Watch”に分類される抗菌薬をなるべく減らそうというのがWHOの打ち出した方針で(“Access”と“Watch”の両方に含まれる薬剤は“Watch”にカウントする)、2023年までに各国が“Access”に分類される抗菌薬を全体の60%以上にするという目標を掲げている。ちなみに、現在、抗菌薬使用量が追跡できている65か国の中で、29か国はすでに60%の数値目標を達成しているようである[7]。
もともとはこの分類は(主として)発展途上国用の必須薬剤リストであったわけだが、2018年1月、抗菌薬適正使用の指標として利用することをSharlandらがLancet Infectious Diseases誌上で提唱し[6]、「AWaRe分類」という名称もこのときに初めて用いられた。AWaReとは、不自然な大文字小文字の配列から想像される通り、“Access”“Watch”“Reserve”の頭文字を取って作られた略語であり、「あわれ」ではなく「アウェアー」と読む(「認知している」という意味の英単語“aware”とも掛けている)。これ以降、WHOにより本分類を利用した国際的な抗菌薬使用量のサーベイランスレポートが出版され[7]、また、本分類を利用して国家間で抗菌薬適正使用を比較した論文が出版され[8]、さらに英国NHSのquality improvementにも本分類が使われたことで[9]、徐々に世界に浸透していった。本分類については2019年6月にWHOにより大々的にキャンペーンが打たれ[10]、今後、世界で抗菌薬適正使用を評価する標準的なツールとなっていくことだろう。
AWaRe分類の課題と展望
とはいえ、この指標にも問題はある。第一に、すべての抗菌薬がAWaRe分類で分けられているわけではなく、未分類(unclassified)の薬剤が多く存在することに注意が必要である。小児用抗菌薬の使用量を国際比較した論文をみると[8]、ベネズエラ、エジプト、バングラデシュでは全体の30%弱の抗菌薬がunclassifiedとなっており、ドイツに至っては35%がunclassifiedである。日本については、この論文では15%程度がunclassifiedの抗菌薬とされている。これは、研究が行われた2015年時点で、本邦で小児によく使用されていたトスフロキサシンやテビペネムが抗菌薬の国際的な分類(Anatomical Therapeutic Classification;ATC)に含まれていなかったためだと考えられる(AMR臨床リファレンスセンターが申請を行い、現在では上記2薬剤はATCに含まれている)。
点有病率調査 (point prevalence survey)により、小児に使用された抗菌薬をAWaRe分類で国際比較した別の論文によると[11]、日本では、新生児敗血症に対してはほとんどunclassifiedの抗菌薬が使用されていないのにもかかわらず、下気道感染症には25%弱のunclassifiedの抗菌薬が使用されているという興味深い状況がみられた。これは、アンピシリン・スルバクタムがAWaRe分類に含まれていないことが影響しているのではないかと思われる。いずれにせよ、unclassifiedの中には非常に広いスペクトラムの抗菌薬(例えば、前述のテビペネム)から非常に狭いスペクトラムの抗菌薬(例えば、トリメトプリム)まで含まれている可能性があり、unclassifiedが多い場合は、その国の抗菌薬の適正性をどう判断してよいものか分からなくなってしまう。
第二に、適応疾患が加味されてないことから、分類の仕方が強引であるという問題もある。マイコプラズマ肺炎や百日咳にはマクロライド(“Watch”)を第一選択薬として使用せざるを得ないだろうし、今後ますます増加が予想されるESBL感染症に対しては、日本国内ではセフメタゾールの使用が適正といえるだろう(第2世代セファロスポリンはunclassified)。また、入院で診るような感染症では、セフォタキシムやセフトリアキソン(いずれも“Watch”)をはじめとした第3世代セファロスポリンを使用する頻度は高い。セフトリアキソンは1日1回投与でよいという簡便さから、在宅医療でも非常に使いやすい抗菌薬であり、日本ではますます使用頻度が高まっていくことが予想される。つまり、“Access”を増やして“Watch”を減らそうという声明があらゆるセッティングにおいて正しいという保証はなく、すべての国のすべての状況に対してこの方針を一律に敷いてしまってよいのかどうかという点には疑問が残る。
第三に、AWaRe分類を使った指標は、抗菌薬の選択のみが反映され、使用量そのものは反映されていないことにもあらためて留意しなければならない。例えば、前述の65か国のデータを見ると、ブラジルの”Access”に分類される抗菌薬の使用比率は60%以上と非常に高い[7]。そのため、AWaRe分類だけをみれば、日本とは比較にならないほど優秀なようだが、ブラジルの抗菌薬使用量自体は2016年時点で22.75 Defined Daily Dose/1,000住民/日(抗菌薬の集計単位については「抗菌薬使用量集計マニュアル」[1]を参照)と、日本(同年で14.60 Defined Daily Dose/1,000住民/日)よりもかなり高い状況にある[12]。AWaRe分類を使って抗菌薬選択の適正性を追求することと、使用量を減少させることは、AMR対策として国の目指すべき車の両輪ととらえなければならないだろう。
ただし、いろいろと課題の多い指標であるとはいえ、“Watch”の薬剤が多く使用されている国(日本を含め)で、“Watch”の抗菌薬が適切に使用されているわけではないだろうことは容易に想像できる。また、“Access”に含まれている抗菌薬ラインナップをみれば、“Watch”から“Access”へのシフトがAMR対策につながるだろうという感覚は誰しもが得られるだろう。また、unclassifiedの問題も将来的には分類自体が見直され、より詳細に抗菌薬が分類された「改訂AWaRe分類」が提唱されることが予想される(それはそれで迷惑な話だが……)。今まで、抗菌薬使用の適正性を抗菌薬使用量の面から判断する指標がなかったため、このAWaRe分類を上手に利用して抗菌薬適正使用に結び付けていくことは重要と言える。
しかし、個人的に思うところを述べるとすれば、日本はAWaRe分類ができる数年前から、“Watch”の大部分を占めると考えられるマクロライド、フルオロキノロン、(第3世代)セファロスポリンに対して、アクションプランで減少させることを目標に頑張ってきた。そのため、あらためてWHOからAWaRe分類の“Watch”を減らすようなキャンペーンを張られると、頑張って宿題をやっているところで母親から「あんた、宿題やってるの?」と言われたような、なんとも釈然としない感覚があるのである。
【References】
1)AMR臨床リファレンスセンター: サーベイランス.
http://amrcrc.ncgm.go.jp/surveillance/index.html
2)厚生労働省: レセプト情報・特定健診等情報の提供に関するホームページ.
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/
kenkou_iryou/iryouhoken/reseputo/index.html
3)WHO: Lessons learnt during 20 years of the Swedish strategic programme against antibiotic resistance.
http://www.who.int/bulletin/volumes/95/11/16-184374/en/
4)Andre M, Molstad S, Lundborg CS, et al; Swedish Study Group on Antibiotic Use: Management of urinary tract infections in primary care: a repeated 1-week diagnosis-prescribing study in five counties in Sweden in 2000 and 2002. Scand J Infect Dis. 2004; 36(2): 134-8.
5)WHO: WHO Model Lists of Essential Medicines.
http://www.who.int/medicines/publications/
essentialmedicines/en/
6)Sharland M, Pulcini C, Harbarth S, et al; 21st WHO Expert Committee on Selection and Use of Essential Medicines: Classifying antibiotics in the WHO Essential Medicines List for optimal use-be AWaRe. Lancet Infect Dis. 2018 Jan; 18(1): 18-20.
7)WHO: WHO Report on Surveillance of Antibiotic Consumption
https://www.who.int/medicines/areas/rational_use/
oms-amr-amc-report-2016-2018/en/
8)Hsia Y, Sharland M, Jackson C, et al: Consumption of oral antibiotic formulations for young children according to the WHO Access, Watch, Reserve (AWaRe) antibiotic groups: an analysis of sales data from 70 middle-income and high-income countries. Lancet Infect Dis. 2019 Jan; 19(1): 67-75.
9)GOV.UK: English surveillance programme for antimicrobial utilisation and resistance (ESPAUR) report.
https://www.gov.uk/government/publications/
english-surveillance-programme-antimicrobial-
utilisation-and-resistance-espaur-report
10)WHO: In the face of slow progress, WHO offers a new tool and sets a target to accelerate action against antimicrobial resistance.
https://www.who.int/news-room/detail/18-06-2019-
in-the-face-of-slow-progress-who-offers-a-new-tool-
and-sets-a-target-to-accelerate-action-against-antimicrobial-resistance
11)Hsia Y, Lee BR, Versporten A et al. Use of the WHO Access, Watch, and Reserve classification to define patterns of hospital antibiotic use (AWaRe): an analysis of paediatric survey data from 56 countries. Lancet Glob Health. 2019;7:e861-e871.
12)WHO: WHO Report on Surveillance of Antibiotic Consumption.
http://www.who.int/medicines/areas/rational_use/
oms-amr-amc-report-2016-2018/en/