ステロイド内服中の髄膜炎、その裏には…(3/3)
最後に糞線虫症に関して概説します。
機 序
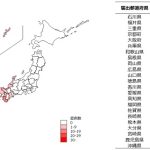
糞線虫症は、糞線虫(Strongyloides stercoralis )によって引き起こされる蠕虫感染症です。糞線虫は熱帯や亜熱帯地域に広く分布し、日本では九州南部、特に鹿児島や奄美大島、沖縄にかけて多く認められます。九州以北での症例の場合は、本症例のようにこれらの地方の出身、あるいは長期の滞在歴があることが多いです(そのほか、戦争などでアジアの熱帯地域に赴いていたなど)。
糞線虫の生活環(図)としては、まず土壌(特に人糞を用いた肥料など)にいるフィラリア型幼虫(以下、F型幼虫)が経皮的に感染し、静脈・リンパ系に侵入して肺胞に到達します(ここで肺炎や喘息様の症状を呈することがあります)。

その後、肺毛細血管を突き破り気道を逆行して嚥下に伴い消化管に侵入し、十二指腸・空腸に定着して約2週間で成熟します。さらに腸管内で産卵し、これが孵化して非感染性のラブジチス型幼虫(以下、R型幼虫)となり、糞便と共に肛門から排泄されます。よって、糞便から認められるのは、ほとんどの場合はR型幼虫です。排泄されたR型幼虫は土壌中で再びF型幼虫となり、感染性を有するようになります。
蠕虫感染症としては珍しく自家感染を起こすことも特徴的です。つまりは肛門に至る前に一部がR型→F型幼虫となり、腸粘膜や肛門から再度静脈系に侵入して感染を繰り返すことで自家感染が成立し、これによって何十年にもわたって感染を持続することができます。
また、当症例のようにステロイドなどを使用して免疫能が低下すると、自家感染を起こすF型幼虫が増加し、肺から消化管に寄生して腹痛や下痢などの消化器症状を起こし、さらに重篤化すると今回のような腸閉塞症状や吸収不良症候群をきたします。腸管からF型幼虫が全身に散布され、その過程で腸内細菌が糞線虫と共に血流感染を起こし、敗血症や髄膜炎、肺炎などを起こすことを播種性糞線虫症と呼びます。
今回、髄液から糞線虫は確認できませんでしたが、おそらくは播種性糞線虫症をきたし、その結果として腸球菌による髄膜炎をきたしたものと推測されます。播種性糞線虫症による髄膜炎の症例報告ではE.coli やKlebsiella 属などの腸内細菌が一般的ですが、少ないながらも今回のように腸球菌による髄膜炎の報告も散見されます。
リスクファクター
また、糞線虫症はHTLV-1感染との関連が知られています。HTLV-1感染はIFN-γの産生を誘導し、Th1を介した反応が増強され、逆にTh2を介した反応が減弱し、結果としてIL-4、IL-5、IL-13やIgE、好酸球の産生が減弱し、寄生虫への応答が鈍くなると考えられており、播種性糞線虫症のリスクが上昇します。HTLV-1感染患者は、健常者と比較して糞線虫症のリスクが2倍になるとする報告もあります[1]。また、HTLV-1は母乳からの垂直感染が主な感染経路と考えられていますが、沖縄や鹿児島は全国平均と比較しても抗体保有率が高いことが知られており、気候に加えて、このことも症例数が多い原因と考えられています。
当患者ではHTLV-1抗体は陰性でしたが、おそらくはステロイドを服用していたことが播種性糞線虫症を発症したリスクと考えられます。ステロイド以外に糞線虫症のリスクとなる病態としては、悪性疾患や低栄養、細胞性免疫を抑制する薬剤の使用、TNF-α阻害薬の使用、低γグロブリン血症、骨髄移植や実質臓器移植(ドナーが感染者である場合や、レシピエントが潜在性感染を起こしていた場合)が挙げられます。HIV感染もリスクの一つと考えられますが、それでもHTLV-1感染と比較すればリスクは低いと考えられています。発症までの年数は、今回のように20年以上経過していることも珍しくなく、感染から50年経過してから発症したとする報告[2]もあります。
骨髄・実質臓器移植前や免疫抑制剤を使用する際には、出身地や曝露歴を確認したうえで糞線虫のリスクが認められれば、便の寄生虫検査や抗体検査(SRL)によるスクリーニングを検討してもいいかもしれません。さらに、糞線虫症として合致する症状がある場合はもちろん、そうでなくても移植前などのケースで抗体陽性であればpre-emptiveに治療してしまう場合もあるようです[3]。
症 状
糞線虫症は様々な皮膚症状を起こすことがあります。当初は糞線虫が皮膚に侵入した際にできる掻痒を伴う浮腫や出血斑、蕁麻疹様の皮疹(皮膚幼虫移行症)などを主として下肢に認めることがありますが、たいていの場合この症状に気づくことはありません。慢性化した場合は、虫体が皮下を這った後に蛇行した紅斑(特に殿部)に加えて、さらに全身性に血管浮腫や蕁麻疹が出現したり、播種性糞線虫症をきたすと臍周囲に紫斑を認めることがあります。
また、採血では好酸球が上昇することがありますが、全例で上昇するわけではありません。当症例では過去数年にわたって好酸球上昇と出現消退を繰り返す好酸球浸潤を伴う皮疹のエピソードを認めていましたが、これは慢性の糞線虫感染症による症状であった可能性があります(病理学的に過去の皮膚生検検体から虫体は確認できませんでした)。
診 断
糞線虫症の診断は、虫体を検体で確認することで行ないます。本来は便の検鏡で確認することがゴールドスタンダードです。スメアは検体少量をスライドグラスに乗せるだけで作成できます。当症例のように腸閉塞をきたして排便が得られないような場合は胃液や十二指腸液、さらには肺炎を呈している場合は喀痰検査の検鏡検査で確認します。ただし、決して感度が良い検査ではありませんので(糞線虫は間欠的に排便から排泄されるため)、何度も繰り返してやっと確認できることもあります。
高い感度で糞線虫を同定する検査としては、寒天平板培養法が知られています。これは「培養」とは名が付くものの、実際には糞線虫を培養するわけではなく、便を乗せた平板を室温(28℃)で2日間保温すると、便中の糞線虫が平板の上を這って回り、それに沿って糞線虫に付着していた便内の腸内細菌がコロニーを形成するのを確認する検査です。ただし、この方法は時間を要するため、検鏡では確認できないけれど播種性糞線虫症を疑うような場合には、この培養法による診断確定を待つのではなく、直ちに治療開始するほうが賢明です。
治 療
通常の糞線虫症の場合は、イベルメクチン200μg/kgを単回投与します。ただし、虫卵へは無効なため、2週間後にもう一度同量内服させることが一般的です。イベルメクチン以外にはアルベンダゾールが使用されることもありますが、その場合は専門家に相談するほうがよいでしょう。
播種性糞線虫症の治療に関しては定説がありません。イベルメクチンを5~7日間継続して使用したり、週1回×4回として使用することもあります。また、アルベンダゾールと併用する場合もあります。
免疫抑制剤を使用している場合は、可能な限りその薬剤の減量や中断も重要です。免疫抑制剤の減量が不可能な場合は、症状が改善するか排便からの排泄の消失が確認できるまで、あるいは(一つの自家感染サイクルである)最低2週間は投与することが一般的です。
当症例のように腸閉塞をきたして消化管への十分な到達や吸収が期待できない場合はさらに問題です。そのような場合は、イベルメクチンの皮下投与や直腸からの浣腸での投与も検討されます。ただし、このような場合も専門家に相談するほうがよいでしょう。
以上、糞線虫に関して概説しました。
本症例を経験して、やはり詳細な病歴聴取が重要であることを再確認しました(今回は出身地がキーポイントでした)。原因不明の好酸球上昇や皮疹、肺炎、消化器症状(特に上部)、腸内細菌による菌血症や髄膜炎を繰り返しているような患者を経験した場合は、ぜひ出身地を確認してみてください。
※タイトルに関しては、○に「ち」を入れてもらえると……。汚くてすみません(汗)。
【References】
1)Hirata T,Uchima N,Kishimoto K,et al:Impairment of host immune response against strongyloides stercoralis by human T cell lymphotropic virus type 1 infection.Am J Trop Med Hyg.2006 Feb;74(2):246-9.
2)Genta RM,Weesner R,Douce RW,et al:Strongyloidiasis in US veterans of the Vietnam and other wars.JAMA.1987 Jul 3;258(1):49-52.
3)Roberta Lattes,et al:Parasites after hematopoietic stem cell or solid organ transplantation,Transplant Infections 3rd ed.,Raleigh A Bowden,et al eds,Lippincott Williams & Wilkins,2010,p. 641-42.
(了)