小児における血液培養検査
はじめに
COVID-19のパンデミックで成人感染症分野が大変な状況になっている。一方、小児分野ではそれほど大きな問題になっていないのに加え、接触機会の減少や感染対策の普及によりむしろ感染症が激減し、なぜか尿路感染症までもが減少する事態となっている[1]。小児感染症医たちは皆、心のどこかに「成人感染症医に申し訳ない」という気持ちを抱えつつ、COVID-19が小児で大きな問題になったときに備え、気持ちを切らさないよう頑張っているはずである。
ところで、世の中はCOVID-19の話題一色であるが、それによって他の感染症に関する知識のアップデートが不要になったというわけではない。ただ単に、その分の勉強量や仕事量が余計に増えただけである。SARS-CoV-2は各地で医療崩壊を引き起こしただけでなく、われわれの脳のキャパシティーをも崩壊させているといえる。
今回、私は小児における血液培養検査の特殊性について、COVID-19で心身ともに疲れている先生方の心に届くよう、努めてナラティブに、ここにまとめた。小児における血液培養検査は、成人感染症医の間だけでなく、小児科医の間でも謎に包まれている。分かっていないことが多い分野なのである。読者がこれを読んで、少しでも小児血液培養に対する理解を深めていただければ幸いである。
小児の血液培養はなぜ1セットでよいのか
成人の血液培養は1セットではなく、2セット採取を原則とする。そうでないと感度が不足し、菌血症を見逃す可能性があるからである。しかし、成人とは異なり、小児の場合、血液培養は基本的に1セット採取であることを知っているだろうか。 たとえば、2018年にアップデートされた米国感染症学会と米国微生物学会の合同ガイドラインでは、小児の血液培養について「好気ボトルを1〜2本、必要に応じて嫌気培養を追加」と記載されており、これを読む限り、1セット採取でも構わないと受け取ることができる[2]。
そして実際、小児科領域では多くの場合、細菌感染症が疑われていても血液培養は当たり前のように1セットしか採取されない[3]。例えば、輸血をする際には、患者の確認はダブルチェックで行うことが一般的である。この場合、小児はシングルチェックで確認してもよいということにはならない。なぜなら、ダブルチェックは確認の精度を上げるために行うもので、その必要性は成人であっても小児であっても同じことだからである。血液培養は、これとどう違うのだろう。成人では検査精度を上げるために2セット行うのに、小児ではそれを行わなくてよいというのは、何かしら奇妙なことのように感じる。
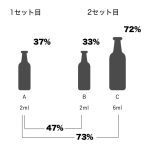
「小児の血液培養は1セットでよい」の元となった根拠はおそらく、1996年に発表されたIsaacmanらの研究である(これは、PUFFYが「アジアの純真」でデビューした年まで遡らなければならないことを意味する)[4]。Isaacmanらの研究は、小児から2セット血液を採取し、それを数本のボトルに分けて注入して培養するというシンプルなものであった。1セット目は2mL採取し、そのすべてをボトルAへ。2セット目は9.5mL採取し、2mLをボトルB、6mLをボトルCへ(残りは定量培養のボトルへ)注入した。すると、ボトルAとボトルBを組み合わせるよりも、ボトルCを単独で用いたほうが細菌の同定率が高かったのである(図)。
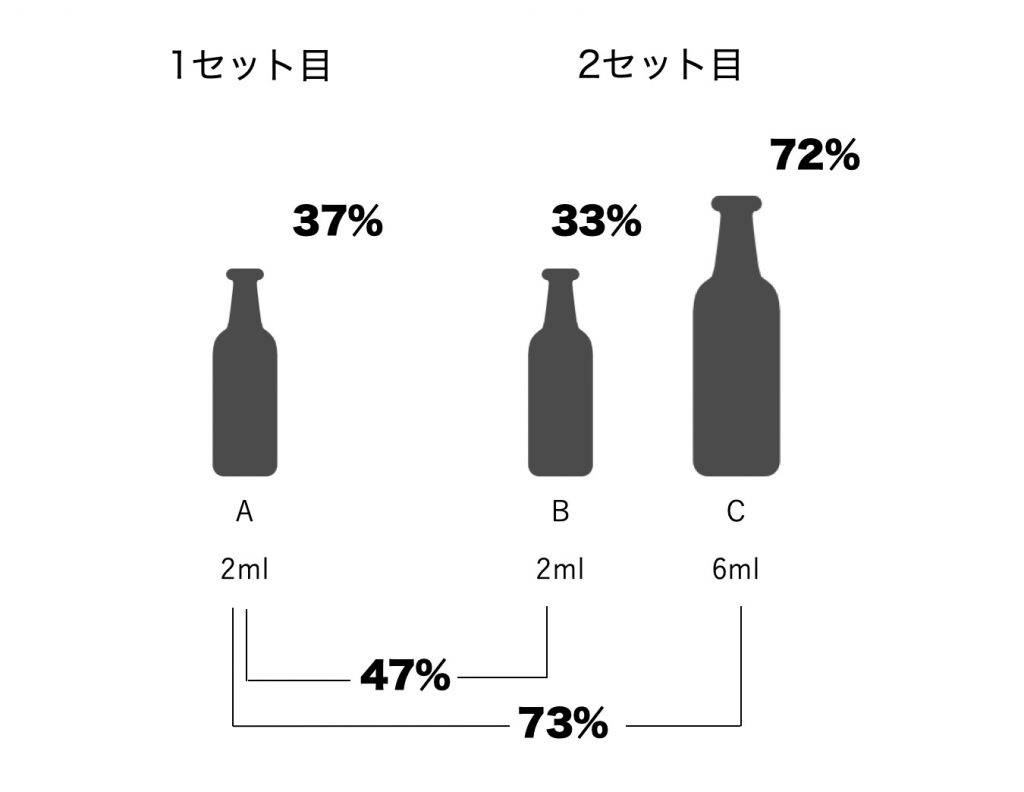
太字は検出率を表す。
検出率は、2mLの血液培養の組み合わせよりも、6mLの血液培養1本のほうが高かった。
しかし、懸命なる読者はすでにお気付きの通り、この研究は「小児の血液培養では、2セット採取することよりも量を確保することが大事である」ことを示唆しているだけで、「小児では1セット採取でよい」ことを示唆しているわけではない。ボトルAとBを組み合わせたほうがボトルA、B単独で判断した場合よりも細菌の検出率が高かったことから、見方を変えれば、少量の場合は2セット採取したほうがよいという結果にも受け取れる。それにもかかわらず、「小児は血液培養1セット」という考えは、この後、広く普及していくこととなる。小児の血液培養における「セット数問題」は、この後も何度か取り組まれ、1セットよりも複数セットのほうが検査感度は良かったという研究結果がいくつか報告された[5、6]。しかし、いずれの報告も採取された血液量が明らかにされておらず、「もし、十分な血液量が確保されていたらセット数の差による違いはなかったのではないか」という疑念は払拭されなかった。
小児で2セット採取が普及しないのには、エビデンスがないこと以外にもおそらく理由がある。それは、小児の採血を何度もやりたくないという他愛もない理由である。かくいう私も、小児に血液培養2セット採取なんてなるべくやりたくはない。それは、小児は血液量が少ないからでも、血管が見つかりづらいからでもなく、ただ単に、彼/彼女らが暴れて大変だからである。
現場の意識とガイドラインの乖離、そして不足するエビデンス
一方、小児の血液培養の検出感度が採取量に左右されるということは多くの研究で報告されており、ほぼ確実と考えられている[7]。しかし、多くの小児科医は血液培養の採取量にこだわっているわけではない[8]。それはなぜだろうか。ここで、米国微生物学会が発行している血液培養ガイドライン(Cumitechガイドライン)が推奨している小児の血液培養採取量を紹介しようと思う[9]。このガイドラインには、体重が2kgを超えている場合(未熟児サイズである)は合計6mL、体重が12.8kgを超えている場合(だいたい2歳くらいである)は合計20mL、36.3kgを超えている場合(だいたい10歳くらいである)は40~60mL採取すると記載されている(表)。
| 体重(kg) | 小児の総血液量(mL) | 採取血液量(mL) | 合計採取血液量(mL) | 合計血液量に占める採血量の割合(%) | |
| 1本目 | 2本目 | ||||
| ≦1 | 50-99 | 2 | – | 2 | 4 |
| 1.1-2 | 100-200 | 2 | 2 | 4 | 4 |
| 2.1-12.7 | >200 | 4 | 2 | 6 | 3 |
| 12.8-36.3 | >800 | 10 | 10 | 20 | 2.5 |
| >36.3 | >2200 | 20-30 | 20-30 | 40-60 | 1.8-2.7 |
(文献9より引用改変)
これはよく言えば非常に厳格な、よく言わなければ、まず不可能な採取量である。2歳児から血液培養のためだけに20mLシリンジで採血している自分自身の姿を、いったいどの小児科医が想像できるだろう。このような実現性の低い血液培養採取量の推奨が現場に受け入れられず、採取量に対する意識低下の原因の一端となっているのは想像にかたくない。それもこれも、すべては小児の血液培養に関するエビデンスの少なさに由来するのだと思う。2002年、Butteryは小児血液培養のレビューで「小児の血液培養に関するエビデンスのほとんどは成人分野からの外挿である」と述べたが[10]、この状況はそれから20年経過した今でもそう大きくは変わっていない。
実際、小児科医の血液培養に対する意識はどうなのか
「小児用血液培養ボトルは嫌気性菌も生える」「血液ボトルにはボトルの色が変わる程度の血液が入ればよい」――。これらは、実際に私が先輩医師から習った、誤った血液培養に関する知識である。今ではそのような間違った知識は払拭されていると信じたいが、やはり小児分野の血液培養に対する関心は高くはなく、あったとしても成人領域の後追いである感がぬぐえない。確かに、血液培養の重要性については小児科医の間でも以前よりはるかに浸透した。採取時のお作法も(本当に必要なのか疑わしいものばかりだが)把握できている。汚染菌の見分け方も、最小発育阻止濃度の見方もだいぶ知識として知られるようになった。しかし、「成人ではそれでよいが、小児でもそれでよいのか」と聞かれると、急に分からなくなるというのが本音のところではないかと思う。「小児は大人のミニチュアではない」という言葉をほとんどの小児科医が訓言として抱えているにもかかわらず、血液培養に関しては成人のやり方をそのまま外挿しているところが大きいのである。
私が所属している、血液培養に関わるとあるグループで、小児の血液培養についてのアンケート調査をしたことがある。患児一人ひとりについて、以下の項目を尋ねた。
(1)適切にボトルを選択したか?
(2)適切に皮膚消毒をしたか?
(3)適切な血液量を採取したか?
2018年の調査で、これらの質問に対して「はい」と答えた割合は、それぞれ(1)99.5%、(2)99.5%、(3)99.8%であった。非常に素晴らしい数字だが、これはいくらなんでも高「すぎる」。このようにアンケート調査で異常に高い数字が出てしまったときは、多くの場合、設問に問題がある。つまり、「適切」という言葉の意味合いが、回答者の間で共有できていなかったのだ。例えば、「適切に処理せよ」という言葉は、飲食店なら「今すぐ掃除しろ」という意味になり得るし、ビジネスシーンなら「株をすべて売り払え」という意味にもなり得る。時と場合によっては、「地の果てまで追いかけて殺せ」という意味になることだってあるかもしれない。このアンケート調査でここまで高い数字が出てしまったことは、回答者の間で小児の血液培養における「適切」という概念がまるで定まっていないことの裏返しでもある。われわれは、小児血液培養における「適切」の定義を必要としているのである。
変わりゆく小児菌血症疫学
1973年、元気に救急外来まで歩いてくる小児の中に、菌血症の児が一定数混じっていることが報告された[11]。この病態はoccult bacteremiaと名付けられたが、このうち一部が髄膜炎などの重症感染症につながることが分かったため[12]、元気な小児であっても月齢や白血球数などから(つまり、血液検査をしなければならないということである!)菌血症の可能性を推定し、セフトリアキソンを一発落とすことが必要とされる時代があった[13、14]。しかし、この厄介な病態については、原因菌が肺炎球菌(約80%)とインフルエンザ菌(約20%)にほぼ限られていたため、世界から消えていくことになる。ヒブワクチンと肺炎球菌結合型ワクチンの普及以降、健康な小児ではoccult bacteremiaを考慮する必要がまずなくなった[15]。この2菌種はoccult bacteremiaに限らず、小児の菌血症の原因の多くを占めていたため、ワクチンによって小児の菌血症疫学は劇的に変化し、現在、血液培養で最も頻繁に検出される細菌は圧倒的に「コンタミネーション」となった[16、17]。
私は、とある市中病院で、小児血液培養の研究を行ったことがある。当時、あまりの血液培養の施行率の低さを改善しようと思い立ち、実際にメルボルンの小児病院で血液培養のプラクティス改善を行ったConnelらの文献を参考に、小児科内で血液培養採取を推進するキャンペーンを張ったのである[18、19]。とても協力的だった後輩たちのおかげもあり、私たちは新興自動車メーカーの販売員のようにひたすら血液培養を採りまくった。その結果、1000患者・日当たりの血液培養採取数は49から107に、陽性率も0.33%から0.81%に上昇した。そして、こう思ったのである。「この0.81%のために、ここまで血液培養をする必要はあったのか?」
これは成人分野にも当てはまることのように思うのだが、検査は、「適切な適応に対して」「適切な方法で採取したサンプルを」「適切な方法で検査し」「適切に解釈する」という4ステップについて「適切とは何か」を定義し、その質を向上させていく必要がある。確かに血液培養の重要性は普及し、医師の他にも看護師や臨床検査技師など多くの職種の貢献により、検査手技や解釈の質、精度は以前よりはるかに向上した。しかし、われわれは最初の関門である「適応」について、あまり深く追い求めてこなかったのではないだろうか。Choosing Wisely運動による検査のスマート化が起きている中、血液検査だけは「多くやるほどよい」というような姿勢が取られてきたのではないか。実は、これに逆行し、本当に必要な人だけから血液培養を採取しようとする動きが小児科から起こってきている(成人分野の追従からの脱却!)。あまりの事前確率の低さ、偽陽性の多さから、血液培養の適応を見直そうという動きがみられてきたのである[20]。
「適切」を明らかにする作業の重要性
長々と小児血液培養について語らせていただいたが、簡単にまとめれば、小児の血液培養はエビデンスに乏しく、それにもかかわらず疫学などの特殊性が強く、さらに既存のガイドラインがあまり有用でない、ということになる。「小児における適切な血液培養」の「適切」を明らかにする作業を行うことが強く求められている状況なのである。
このことを受けて、私と、広島大学の志馬伸朗先生、兵庫県立こども病院の笠井正志先生、兵庫県立尼崎総合医療センターの伊藤雄介先生、あいち小児保健医療総合センターの伊藤健太先生、国立循環器病研究センターの福田修先生、京都府立医科大学附属病院の山田幸司先生は、「こどもの血液培養と菌血症カレッジ」を立ち上げ、2017年より小児における血液培養検査の標準化に取り組んでいる(このグループはKOKETSUKINという略称でアカデミアの世界にも登録されている[8])。
レクチャーを主な活動とするが、「適切」を明らかにするためのチェックリストを公開できたことは、小児における血液培養標準化のための大きな一歩であると考えている[21]。現在、Johns Hopkins Children’s Centerなどを中心として、これとほぼ同様の取り組みが進行しているようだが[22]、(誰が何と言おうと!)公開はこちらのほうが先である。小児血液培養の実践にあまり自信のない病院、標準化のやり方に困っている病院などがあったら、ぜひ、われわれの作成したチェックリストをダウンロードして参考にしていただきたい。本当は、この記事上でチェックリストについて紹介する予定だったのだが、前置きに等しい内容だけで埋め尽くしてしまった。もし、またの機会があれば、チェックリストの内容を紹介させていただければ幸いである。
COI開示:執筆者のCOIは特になし。
【References】
1)Hatoun J, Correa ET, Donahue SMA, et al: Social Distancing for COVID-19 and Diagnoses of Other Infectious Diseases in Children. Pediatrics. 2020 Oct; 146(4): e2020006460.
2)Miller JM, Binnicker MJ, Campbell S, et al: A Guide to Utilization of the Microbiology Laboratory for Diagnosis of Infectious Diseases: 2018 Update by the Infectious Diseases Society of America and the American Society for Microbiology. Clin Infect Dis. 2018 Aug 31; 67(6): e1-94.
3)笠井正志, 志馬伸朗, 川口 敦: 小児集中治療室における血液培養採取の現状. 日集中医誌. 2014; 21: 55-6.
4)Isaacman DJ, Karasic RB, Reynolds EA, et al: Effect of number of blood cultures and volume of blood on detection of bacteremia in children. J Pediatr. 1996 Feb; 128(2): 190-5.
5)Kaditis AG, O’Marcaigh AS, Rhodes KH, et al: Yield of positive blood cultures in pediatric oncology patients by a new method of blood culture collection. Pediatr Infect Dis J. 1996 Jul; 15(7): 615-20.
6)Wattier RL, Dvorak CC, Auerbach AD, et al: Repeat blood cultures in children with persistent fever and neutropenia: Diagnostic and clinical implications. Pediatr Blood Cancer. 2015 Aug; 62(8): 1421-6.
7)Huber S, Hetzer B, Crazzolara R, et al: The correct blood volume for paediatric blood cultures: a conundrum? Clin Microbiol Infect. 2020 Feb; 26(2): 168-73.
8)Kusama Y, Shime N, Ito K, et al. The Volume of Pediatric Blood Culture. Pediatr Infect Dis J. 2019 Dec; 38(12): e340-1.
9)Baron EJ, MP Weinstein, Dunne WM Jr, et al: Cumitech 1C, Blood Culture IV. ASM Press, Washington, DC, 2005.
10)Buttery JP: Blood cultures in newborns and children: optimising an everyday test. Arch Dis Child Fetal Neonatal Ed. 2002 Jul; 87(1): F25-8.
11)McGowan JE Jr, Bratton L, Klein JO, et al: Bacteremia in febrile children seen in a “walk-in” pediatric clinic. N Engl J Med. 1973 Jun 21; 288(25): 1309-12.
12)Shapiro ED, Aaron NH, Wald ER, et al: Risk factors for development of bacterial meningitis among children with occult bacteremia. J Pediatr. 1986 Jul; 109(1): 15-9.
13)Kuppermann N, Fleisher GR, Jaffe DM: Predictors of occult pneumococcal bacteremia in young febrile children. Ann Emerg Med. 1998 Jun; 31(6): 679-87.
14)Baraff LJ, Oslund S, Prather M: Effect of antibiotic therapy and etiologic microorganism on the risk of bacterial meningitis in children with occult bacteremia. Pediatrics. 1993 Jul; 92(1): 140-3.
15)Stoll ML, Rubin LG: Incidence of occult bacteremia among highly febrile young children in the era of the pneumococcal conjugate vaccine: a study from a Children’s Hospital Emergency Department and Urgent Care Center. Arch Pediatr Adolesc Med. 2004 Jul; 158(7): 671-5.
16)Greenhow TL, Hung YY, Herz A: Bacteremia in Children 3 to 36 Months Old After Introduction of Conjugated Pneumococcal Vaccines. Pediatrics. 2017 Apr; 139(4): e20162098.
17)Sard B, Bailey MC, Vinci R: An analysis of pediatric blood cultures in the postpneumococcal conjugate vaccine era in a community hospital emergency department. Pediatr Emerg Care. 2006 May; 22(5): 295-300.
18)Connell TG, Rele M, Cowley D, et al: How reliable is a negative blood culture result? Volume of blood submitted for culture in routine practice in a children’s hospital. Pediatrics. 2007 May; 119(5): 891-6.
19)千葉浩介, 日馬由貴, 古河賢太郎・他: 血液培養採取指針の作成による菌血症検出率変化の検討. 日小児救急医会誌. 2017; 16: 431-4.
20)Woods-Hill CZ, Fackler J, Nelson McMillan K, et al: Association of a Clinical Practice Guideline With Blood Culture Use in Critically Ill Children. JAMA Pediatr. 2017 Feb 1; 171(2): 157-64.
21)こどもの血液培養と菌血症カレッジ: 小児血液培養採取チェックリスト.
http://www.bdj.co.jp/micro/ketsubai/koketsukin-checklist.html
22)Johns Hopkins Children’s Center: Bright STAR Collaborative.
https://www.hopkinsmedicine.org/johns-hopkins-childrens-center/what-we-treat/specialties/infectious-diseases/programs-centers/bright-star/