【ミニレビュー】
βラクタム系抗菌薬アレルギー
(Q&A形式でみる)
| Q1:「以前にβラクタム系薬でアレルギーがあった」と言われた場合、他系統のβラクタム系薬については、慎重に経過をフォローしながら使用してよいのか? それとも避けるべきなのか? A1:他系統のβラクタム系薬使用の可否は、認めたアレルギーの重症度やタイプによって判断をする。そのためには、以前のアレルギーに関してしっかりとした問診を行うことが必要となる。アレルギーがアナフィラキシーや重症薬疹(「補足:重症薬疹について」参照)であった場合には、すべてのβラクタム系薬を避けることが望ましい。 |
[解説]
薬剤過敏症(hypersensitivity reactions;HSRs)は、免疫学的反応であるアレルギーと、非免疫学的反応であり症状がアレルギーと類似した偽アレルギーに分けることができる。最初にこの2群に分類する。
さらに前者のアレルギーは、その病態によって4つに分類することができる。古典的にはGellとCoombsの分類(表1)1)が用いられる。
表1 GellとCoombsの分類| タイプ | Ⅰ型 | Ⅱ型 | Ⅲ型 | Ⅳ型 |
| 原因 | IgE | IgG(抗体) | 補体 | T細胞活性化 |
| 発症時期 | 主に1時間以内 | 7~14日 | 7~14日 | 以下に記載 |
| 臨床症状 | アナフィラキシー、蕁麻疹、血管浮腫 | 溶血性貧血、血小板減少症、好中球減少症 | 血清病、血管炎 | |
| 原因となる主な抗菌薬 | ペニシリン、セファロスポリン,フルオロキノロン | ペニシリン、セファロスポリン、スルファメトキサゾール | セファロスポリン(特にセファクロル)、シプロフロキサシン、ペニシリン、スルファメトキサゾール |
| タイプ | IVa | IVb | IVc | IVd |
| 原因 | Th1、IFN-γ | Th2 | CD8 | T-cell(IL8) |
| 発症時期 | 10~15日 | 2~8週間 | 4~28日 | 24~48時間 |
| 臨床症状 | 接触性皮膚炎 | DIHS & DRESS | SJS & TEN | AGEP |
| 原因となる主な抗菌薬 | 局所抗菌薬 | ペニシリン、セファロスポリン、ダプソン、ミノサイクリン、スルファメトキサゾール、バンコマイシン | フルオロキノロン、ペニシリン、スルファメトキサゾール | アンピシリン、抗真菌薬、フルオロキノロン、スルファメトキサゾール |
主な重症薬疹では、原因となる薬剤、発生機序、発生時期、症状などが異なるため、それぞれの鑑別が重要となってくる。抗菌薬による重症薬疹は、他の薬剤によるものと比べて早期に発症することがある。
※補足:重症薬疹について| それぞれの重症薬疹について、厚生労働省「重篤副作用疾患別対応マニュアル」をもとに解説する。 ● 薬剤性過敏症症候群 (drug-induced hypersensitivity syndrome;DIHS)2)、 (drug reaction with eosinophilia and systemic symptoms;DRESS) 1) 早期に認められる症状 紅斑に加え、発熱(38℃以上)、咽頭痛、全身倦怠感、食欲不振などの感冒様症状、リンパ節腫脹 2) 副作用の好発時期 原因医薬品の服用後2~6週間以内に発症することが多いが、数年間服用後に発症することもある。 3) 推定原因医薬品 比較的限られており、主にカルバマゼピン、フェニトイン、フェノバルビタール、ゾニサミド(抗てんかん薬)、アロプリノール(痛風治療薬)、サラゾスルファピリジン(サルファ剤)、ジアフェニルスルホン(抗ハンセン病薬)、メキシレチン(不整脈治療薬)、ミノサイクリン(抗生物質)などがある。 解説:DIHSとDRESSの違いは、DIHSはHHV6の再活性化に重点を置き、DRESSは好酸球の上昇に重点を置いていることである。これらが他の重症薬疹と違っている点は、2週間以上経過しての発症が多いこと、原因薬剤が限られていることである。 ●スティーヴンス・ジョンソン症候群(Stevens-Johnson syndrome;SJS)3)、 中毒性表皮壊死融解症(toxic epidermal necrolysis;TEN)4) 1) 早期に認められる症状 発熱(38 ℃以上)、眼の充血、眼脂(眼分泌物)、まぶたの腫れ、目が開けづらい、口唇や陰部のびらん、咽頭痛、紅斑 2) 副作用の好発時期 原因医薬品の服用後2週間以内に発症することが多いが、数日以内あるいは1か月以上のこともある。なお、眼病変は、皮膚または他の部位の粘膜病変とほぼ同時に、あるいは皮膚病変より半日ないし1日程度先行して認められ、両眼性の急性結膜炎を生じる。 3) 推定原因医薬品 抗菌薬、解熱消炎鎮痛薬、抗けいれん薬、痛風治療薬、サルファ剤、消化性潰瘍薬、催眠鎮静薬・抗不安薬、精神神経用薬、緑内障治療薬、筋弛緩薬、高血圧治療薬など広範囲にわたり、その他の医薬品によっても発生することが報告されている。 解説:多くの薬剤が原因となる重症薬疹である。発熱や多形紅斑様皮疹、びらんを伴うことが多いが、まれに粘膜病変のみのSJSもある。粘膜病変が10%以内のものがSJS、10%を超えるものがTENと診断され、TENはSJSからの進行が大部分を占める。 ●急性汎発性発疹性膿疱症(acute generalized exanthematous pustulosis;AGEP)5) 1) 早期に認められる症状 医薬品服用後、急速に出現する無数の小膿疱を伴うびまん性の紅斑、浮腫性紅斑に加え、発熱(38℃以上)、全身倦怠感、食欲不振 2) 副作用の好発時期 原因医薬品の服用後、数時間~数日以内に発症する場合(すでに薬剤に対して感作されている場合)と、服用後1~2週間後に発症する場合(初めて服用した場合)がある。 3) 推定原因医薬品 ペニシリン系(アンピシリン、アモキシシリン)、マクロライド系(ロキシスロマイシン)、セフェム系(セファロスポリン)、オキサセフェム系(フロモキセフ)、カルバペネム系(イミペネム)、テトラサイクリン系(ミノサイクリン)、キノロン系(ノルフロキサシン、オフロキサシン)、イトラコナゾール、テルビナフィン(抗真菌薬)、アロプリノール(痛風治療薬)、カルバマゼピン(抗てんかん薬)、ジルチアゼム(降圧薬)、アセトアミノフェン(鎮痛解熱薬)などが報告されている。ブフェキサマク含有外用薬や水銀摂取でも発症することがある。 解説:他の重症薬疹に比べて、早期に発症することが特徴である。粘膜疹を認めないことが多い。薬剤中止後、2週間程度で改善することが多い。 なお、ペニシリンやセファロスポリンといったβラクタム系抗菌薬は、即時型アレルギー、どのタイプの重症薬疹の原因にもなり得る。薬歴や発症時期、症状などから判断する必要がある。 |
| Q2:βラクタム系抗菌薬((1)ペニシリン系、(2)セフェム系、(3)カルバペネム系、(4)モノバクタム系)でのアレルギーの特徴は? 交差アレルギーや代替抗菌薬は、どのように考えるか? A2:前述のように、重篤なアレルギーの既往がある場合にはβラクタム系薬以外の抗菌薬を選択すべきであるが、軽微な場合は交差アレルギーの有無を考慮しての使用も検討される。以下に、各系統抗菌薬別に記す。 |
| [βラクタム系抗菌薬全般について]※詳細は文末「追加説明」を参照 βラクタム系抗菌薬を構成するβ-ラクタム環、チアゾリジン/ジヒドロチアジン環、および側鎖はすべて、免疫原性を潜在的に有する6)。しかし、その分解経路の違いによって抗原としての重要性が異なってくる。 |
| [A 2-(1):ペニシリン系について] ペニシリン系薬を避け、セファロスポリン系薬やカルバペネム系薬、もしくはモノバクタム系薬を選択する。ただし、アミノペニシリンは第一世代や第二世代のセファロスポリン(アミノセファロスポリン)との交差アレルギーの可能性があるため、慎重を期するなら第三世代以降のセファロスポリン系薬を選択する。 |
[解説]
1940年代にペニシリンが使用されるようになってまもなく、ペニシリンによるアナフィラキシーが報告されている。ペニシリンアレルギーの有病率は2%程度と考えられており、0.01~0.05%の患者でアナフィラキシーのリスクがある。ペニシリンに対するIgEを介した反応性は年々低下していき、アナフィラキシー反応から 7~12か月後では93%であるが、10年後には22%の患者のみが反応性を認めたと報告されている7)。
ペニシリン系抗菌薬は、その分解過程で蛋白質の残留リジンに結合できる不完全な中間体としてpenicilloylを形成する。penicilloylが蛋白質と結合することにより、抗原となる。この過程から、何らかのペニシリン系抗菌薬にアレルギーがある場合には、他のペニシリン系抗菌薬にも反応する可能性がある。セファロスポリン系抗菌薬ではこのような分解経路をたどらないため、側鎖の違うセファロスポリン系抗菌薬は選択可能である。
ペニシリンアレルギーの既往があると申告された場合には、後述する皮膚試験やチャレンジテストによって使用の可否を検討することもある。
アモキシシリン/クラブラン酸の過敏症では、約30%の患者でクラブラン酸が原因と示唆され たとの報告がある8)。その場合、アモキシシリンは使用可能である。
ワイドシリン®細粒20%製剤は、添加物としてカルミンを含む。そのため、赤色色素のコチニール、カルミンに過敏症のある患者では避けるべきである。2012年5月の厚生労働省からの通達9)に伴い、添付文書への記載の徹底と禁忌項目の改訂が行われている10)。
| [A 2-(2):セファロスポリン系について] R1側鎖の違うセファロスポリン系薬を選択する。セファゾリンは他のセファロスポリン系薬とは交差アレルギーが少ない。第三世代、第四世代セファロスポリン系薬ではR1側鎖の類似による交差アレルギーに注意する。 ただし、異なるR1側鎖を有する複数のセファロスポリン系抗菌薬にアレルギーの既往がある場合は、主構造のβラクタム環が抗原である可能性があるため、βラクタム系薬以外の別系統の抗菌薬を選択すべきである。 |
[解説]
1~3%の患者がセファロスポリン系薬に過敏症であると報告されているが、実際にはそれ以上に申告される傾向にある。アナフィラキシーの頻度は、ペニシリン系薬に比べてかなり低いと考えられる。
セファロスポリン系抗菌薬では、R1側鎖の類似性(文末「追加説明」表3を参照)が即時型・遅延型アレルギーともに重要であると考えられている。
初期のレトロスペクティブ研究では40%程度のペニシリンアレルギー患者で交差アレルギーが起こるとされていたが、近年では過大報告されていたと考えられている。初期(1980年以前)のセファロスポリン系抗菌薬にはトレース量のペニシリンが含まれていたこともあり、過大に報告されていた原因の一つと考えられる。現在、側鎖を共有しないセファロスポリン系薬では、ペニシリン系抗菌薬との交差アレルギーは1~4%と報告されている11)。
世代により頻度に幅があり、第一・二世代セファロスポリンは第三・四世代セファロスポリンに比べて、ペニシリン系抗菌薬との交差アレルギーの頻度が高くなると報告されている。交差アレルギーは前述のように、主にR1側鎖の類似によるものが原因と考えられる。そのため、アミノペニシリンでのアレルギー歴がある患者では、アミノセファロスポリンとの交差アレルギーが起こり得る。これは、第一世代や第二世代での交差アレルギーが多い要因と考えられる。アミノセファロスポリンとペニシリンの交差アレルギーは、約10%と報告されている。
また、ピペラシリンとセフォペラゾンのR1側鎖は類似している(水酸基の有無の違い)。
セファゾリンは第一世代であるが、同一のR1側鎖を持つ他のβラクタム系抗菌薬はない特異的な構造であり(Ceftezole[タイファロゾール®]のみ同一側鎖を有するが、現在は販売されていない)、他のβラクタム系抗菌薬との交差アレルギーは少ないと考えられる。セファゾリンによる過敏反応を示す患者は、他のセファロスポリンやペニシリンに忍容性を示す可能性が示唆されている12)13)。
セフォタキシム、セフトリアキソン、セフェピムは、R1で同一の側鎖構造(メトキシイミノ基)を有するため、交差アレルギーの可能性が高い。
セファロスポリン系薬でのアレルギー歴がある患者では、側鎖の異なるセファロスポリン系薬を考慮する。側鎖の異なるセファロスポリン系薬の皮膚試験陰性は、安全に使用できる指標となる。慎重に判断するなら、これに続きチャレンジテストを行うことが望ましい。しかしながら、明確なアナフィラキシーショックや重症薬疹のような重篤な薬剤過敏症の既往がある場合には、すべてのβラクタム系薬を避け、他系統の薬剤の選択を考慮する。
なお、セファクロルは他のセファロスポリン系薬に比べて薬剤過敏反応が多く、血清病(III型アレルギー)の頻度も高い。同様に黄色ブドウ球菌に有効であるセファレキシンに比べて明らかに頻度が高いため、治療において積極的にセファクロルを選択する理由はない。
| [A 2-(3):カルバペネム系について] ペニシリン系抗菌薬、セファロスポリン系抗菌薬との交差アレルギーは少ないと考える。必要に応じて皮膚試験を行うことは、使用可能と判断する指標となる。 |
[解説]
ペニシリンアレルギーの既往のある患者で、カルバペネム系薬の皮膚試験が陽性となる患者は1%程度である。ペニシリン系抗菌薬、セファロスポリン系抗菌薬ともに、交差アレルギーは1%未満と推定される14)。
IgE介在性ペニシリンアレルギー患者における皮膚試験の陰性確認は、安全にカルバペネム系薬を使用できる指標となる15)。
ペニシリンによるアナフィラキシーまたは非アナフィラキシーを申告した患者110人において、ペニシリン皮膚試験を施行せず1~4週間のメロペネム治療が安全に実施できたとの報告がある16)。
また、ペニシリンアレルギーの申告があった患者となかった患者で統計学的な差はなかったが、申告がなかった患者のほうがカルバペネム系抗菌薬による薬剤過敏症が多かった報告17)があり、ペニシリンアレルギー歴はカルバペネム系抗菌薬による過敏症の推測にはあまり有用でないことが示唆される。しかしながら、このような報告がペニシリンアレルギーと申告された患者へのカルバペネム系薬の使用増に影響してしまうことも懸念される。実際、グラム陰性菌の血流感染において、カルバペネム系抗菌薬が使用される頻度が高いことが報告されている17)。
| [A 2-(4):モノバクタム系について] セフタジジム以外の他のβラクタム系薬との交差アレルギーはほぼないと考えられる。 |
[解説]
アズトレオナムとペニシリン系薬との交差アレルギーはIgE介在性18)・T細胞介在性19)ともに極めて低く、ペニシリン系薬やセファロスポリン系薬によるアレルギーの既往のある患者でも使用できる。ただし、セフタジジムとは側鎖が類似しているためI型アレルギーの交差アレルギーリスクがあり、避けるべきである20)。まれなIgE関連アレルギーの除外では、事前の皮膚試験が有用であるとの報告がある15)。
| Q3:βラクタム系薬でアナフィラキシーショックや重症薬疹となったことがある場合の、感染フォーカスごとの代替抗菌薬の考え方は? A3:リスクが高いアレルギー歴(アナフィラキシーショックや重症薬疹)などでは系統の違う抗菌薬を選択する必要がある。臓器、起因菌、宿主などを考慮した感染症治療の原点に帰る必要がある。このような知識は、セファゾリンの供給不足などの他の場面でも役に立つと考える。以下に、代替抗菌薬について記載する。 |
[解説]
代替抗菌薬は臓器と起因菌を想定して選択する。
例)
誤嚥性肺炎:クリンダマイシン、グラム陽性菌用抗菌薬+メトロニダゾール
尿路感染症:ST合剤、フルオロキノロン、アミノグリコシド
皮膚軟部組織感染症:ST合剤、クリンダマイシン、塩酸バンコマイシン
腹腔内感染症:フルオロキノロン+メトロニダゾール
ペニシリンアレルギー申告患者において臨床現場で問題となる場面は周術期投与であろう。非アナフィラキシー・ペニシリンアレルギー患者では、セファゾリンは安全に使用できる可能性が高いにもかかわらず、約20%の医師がセファゾリンの使用を避けていたという調査がある。本調査では、ペニシリンとセファゾリンの交差アレルギーに対する知識を有する医師は約半数であり、知識の有無がセファゾリン選択に影響していた21)。
また、脱感作療法は一時的な忍容性を高めるだけであり、永久に効果があるものでないことに注意が必要である。
| Q4:ペニシリンアレルギーの診断は、どのようにすればよいか? A4:問診およびそれに続くアレルギー反応試験で行う(表2)14)。 |
問診上、リスクの低い症状としては、家族歴の申告のみや消化器症状、皮疹のない掻痒感、頭痛などの非アレルギー症状の申告となる14)22)。
アレルギー発生時の併用薬の確認をすることも必要である。アロプリノールは重症薬疹での一番の原因薬剤であり、抗けいれん薬は抗菌薬とアレルギーの頻度が近い。また、頻繁に処方されるNSAIDsも薬疹の頻度は高い。これらの薬剤に起因するアレルギーが抗菌薬のものとされることもある。特にIV型アレルギーは原因薬剤を中止しても数日悪化をたどることがあり、原因薬剤の特定が難しくなる。
抗ペニシリン血清学的診断(IgE)によるin vitro検査は臨床症状との相関性が低く、診断には無効とされている23)。I型アレルギーでは皮膚試験や特異的IgE検査(RAST)、IV型アレルギーではパッチテストなどが診断に使用される。
表2 ペニシリンアレルギーの申告があった際に行うべき診断| 低リスク | 中間リスク | 高リスク | |
| History | ・アレルギーの可能性の低い単独の反応(消化器症状や頭痛) ・皮疹のない掻痒感 ・IgE反応を疑わせない不明な過去の反応(>10年前) ・家族のペニシリンアレルギー歴 |
・蕁麻疹または掻痒性皮疹 ・IgE反応を疑うが、アナフィラキシーではない |
・アナフィラキシーの診断 ・皮膚試験の陽性 ・反応の再発 ・複数のβラクタム系抗菌薬に対する反応 |
| Action | ・アモキシシリンの処方または観察下でのアモキシシリンチャレンジテスト | ・皮膚試験が陰性であれば、それに続き観察下でのアモキシシリンチャレンジテスト ・アレルギーや免疫の専門家への紹介 |
・アレルギーや免疫の専門家への紹介または脱感作 |
| ●ペニシリン皮膚試験 プリックテストおよび皮内テストで行われる。 penicilloyl-polylysine(PPL)は、ペニシリンのβラクタム環が開裂されたpenicilloylを重合リシンと結合させたものであり、安全に使用できる試薬として開発された。メジャー決定基の試薬として使用されるが、本邦では販売されていない。マイナー決定基のための試薬はまだ一般的でなく、ペニシリンGを使用する施設が多い。メジャー決定基が陰性でマイナー決定基が陽性だった場合、側鎖が抗原決定基になっている可能性が示唆される。 皮膚試験の陽性適性率は約50%とされている。陽性であった場合には当該薬剤を避けるべきである。 米国では、トレーニングを受けた薬剤師による検査によって、抗菌薬適正使用が推進されたとの報告が出ている23)。 ペニシリンアレルギー歴により他の抗菌薬の使用が多い施設では、皮膚試験の導入は効果的と考えられる。しかし、本邦では試薬が販売されていないため、実薬を使用することになるが、その場合にはアナフィラキシー発生に注意が必要となる。 ペニシリン皮膚試験陽性であっても、R1側鎖が同一でないセファロスポリン系抗菌薬1)、カルバペネム系抗菌薬との交差アレルギーの頻度は低い24)。 以下の患者では皮膚試験は不要である。 ・申告が家族歴のみである患者 ・ペニシリンアレルギーの既往があるが、その後、当該薬剤を問題なく使用できた患者 以下の患者は皮膚試験を行うべきでない。 ・明らかなIgE・IgM反応性アレルギーを起こしたことがある患者 ・重症薬疹の既往がある患者(パッチテストは可能かもしれない) セファロスポリンに対する皮膚試験のエビデンスは、ペニシリンに対するものに比べるとまだ蓄積は少ない。 ●経口チャレンジテスト 少量の実薬を用いて行う検査法であり、アナフィラキシーを起こす可能性があるため、緊急の対応が取れるような体制で行うべきである。場合によっては緊急輸液ができるよう、点滴ルートを確保してから行うことも必要となる。アモキシシリンが使用されることが多い。重症薬疹の既往がある患者ではチャレンジテストは行うべきではない。 |
| ●アレルギーの間違った記録がされないために 正確な薬剤名の記録が必要である。一般に「抗菌薬=ペニシリン」と考える患者は多い。超高齢者の幼少期のアレルギーでは、サルファ剤によるものであってもペニシリンと記憶されている例も考えられる。サルファ剤は遅延型アレルギーによる薬疹の頻度が高いため、そのような事例ではサルファ剤を疑い、ST合剤を避けるべきかもしれない。 余談であるが、いまだに「アスピリン=ピリン系」と勘違いしている患者(および医療従事者)にしばしば遭遇する。筆者は製品名(バファリン®)などで再確認するようにしている。以前販売されていた医療用セデスG®はイソプロピルアンチピリン(ピリン系)を含有する。下痢やめまいのような起こり得る軽微な副反応に関しては、処方時に患者に説明をすることによってアレルギーとの認識が下がると考えられる。 また、DRESSなどでは原因薬剤を中止後も悪化する事例が多い。このような経過も原因薬剤の決定に影響してしまう。前述のようにIgEを介した抗体は年々低下することにより、多くの患者から抗体は消失する。アレルギー歴との乖離の原因の一つである。 ●アレルギーの既往に関する問診:薬剤師である筆者が記録している例 ・原因となった薬剤名は? 商品名まで確認できるように問診を行うことにより、原因薬剤を特定できる可能性が高くなる。あいまいであった場合は特定が困難であるが、軽微だった可能性が示唆される。 ・そのアレルギーはいつごろ起こったのか?(何年前か?) 前述のように、10年を経過すると多くの患者では抗体が消失する。 ・どのような症状であったか? IgEを介したアナフィラキシーの症状でないか判断が必要。記憶に残っていない症状であれば重篤でなかった可能性が高い。 ・原因と考えられる薬剤を飲んでどのくらいの時間で起こったか? 1時間を超えるアレルギーは即時型反応でない可能性が高い。数時間で起こった皮疹は遅延型反応でない可能性が高い(むしろ、それ以前に服用していた薬剤によるものか、即時型反応の表現と考える)。 ・アレルギーのため通院、あるいは救急搬送や入院となったか? 重症度の判断に役立つ。 ・同じ薬剤をそれ以降に使用したことがあるか? ・お薬手帳や紹介状などでアレルギーとされた抗菌薬(および同系統薬)が処方された記録はないか? それを服用した際に何も起こらなかったか? 安全に使用できた抗菌薬は、通常は問題なく使用可能と考える。お薬手帳に記載されていても患者自身が服用しなかったような事例は多々あるため、確実な服用歴を確認しなければならない。 ・アレルギー疾患はあるか? アトピー性皮膚炎はペニシリンアレルギーには影響しないが、喘息は生命を脅かす反応を起こす可能性がある6)。 【独立行政法人医薬品医療機器総合機構(PMDA)への報告および患者被害救済制度】 薬剤過敏症が生じた場合、医療従事者は副作用報告の義務がある。また、副作用救済制度について患者および家族に情報提供することも必要である。詳細はPMDAのウェブサイト(https://www.pmda.go.jp/)を参照。 |
追加説明:βラクタム系薬アレルギーの薬剤側の要因(さらに深く学ぶために)
βラクタム系抗菌薬は、即時型・遅延型両方のアレルギーの原因となる。
βラクタム系抗菌薬は、化学構造的にすべて4員環のβラクタム環を有する。隣接構造が系統別に違っている(図1)11)。
・ペニシリン系抗菌薬:5員環のチアゾリジン環および側鎖を1つ(R1)持つ。
・セファロスポリン系抗菌薬:6員環のジヒドロチアジン環および側鎖を2つ(R1、R2)持つ。
・カルバペネム系抗菌薬:ペニシリンとやや異なる構造のチアゾリジン環を持つ。
・モノバクタム系抗菌薬:隣接環を有さない。
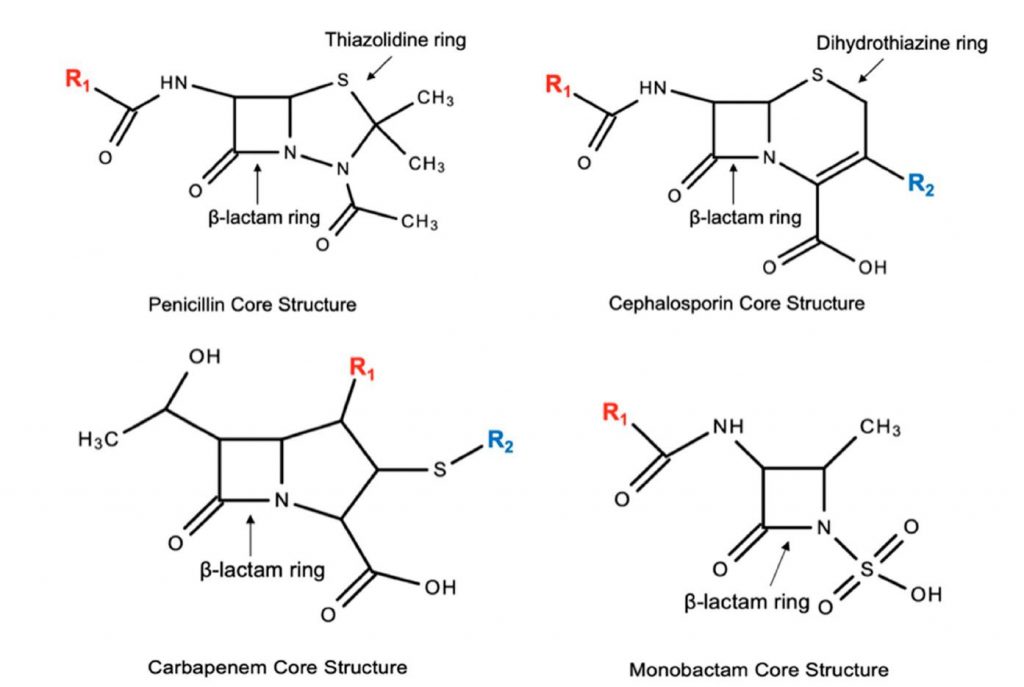
(文献11より引用)
β-ラクタム環、チアゾリジン/ジヒドロチアジン環、および側鎖はすべて、免疫原性を潜在的に有する6)。組織や血清中の蛋白質と結合して、ハプテンとして作用することにより抗原性を示す。
ペニシリン系抗菌薬とセファロスポリン系抗菌薬は構造に類似点があるが、その分解経路が異なる(表3)25)。ペニシリン系は蛋白質の残留リジンに結合できる不完全な中間体としてpenicilloylを形成して抗原となる。セファロスポリン系抗菌薬は速やかにフラグメントに分解され、分解生成物の免疫原性がそれほど強くないことがペニシリン系抗菌薬とは異なる。一方、R1側鎖は構造を残したまま分解されるため、抗原決定構造となる。
米国では約10%の患者がペニシリンアレルギーと申告しており、高齢者や入院患者でその頻度が高まる。そのうち約90%の患者では安全に投与することができると報告されている26)。過剰なペニシリンアレルギー診断は、高価で不適切な抗菌薬使用を助長する27)。また、入院期間の延長やC. difficile、MRSA、VRE感染症のリスクも高まることが報告されている28)。
また、アレルギー歴の申告は抗菌薬の選択に影響を与える。MSSA菌血症ではペニシリンアレルギーの申告は生存率に影響しなかったが、多くのアレルギーとされる患者はセファゾリンの治療を受け、バンコマイシンが選択された群での死亡率の上昇がみられたため、適切なセファゾリンの選択が有効であると報告されている29)。
表3 R1側鎖の類似| A | B | C |
| Benzylpenicillin (Penicillin G) Cephaloridine Cephalothin Cefoxitin(マーキシン®) |
Amoxicillin(サワシリン®) Cefadroxil(サマセフ®) Cefprozil Cefatrizine(セプチコール®) |
Ampicillin(ビクシリン®) Cefaclor(ケフラール®) Cephalexin(ケフレックス®) Cephradine Cephaloglycin Loracarbef |
| D | E | F |
| Ceftriaxone(ロセフィン®) Cefotaxime(クラフォラン®、セフォタックス®) Cefpodoxime(バナン®) Cefditoren(メイアクト®) Cefmenoxime(ベストコール®) Cefepime(マキシピーム®) Cefpirome(ブロアクト®、ケイテン®) |
Ceftazidime(モダシン®) Aztreonam(アザクタム®) |
Cefazolin(セファメジン®) |
(文献25より引用)
アミノペニシリンとアミノセファロスポリン(セファレキシン、セファクロル、セファドロキシル)は同一R1側鎖を有すため、IgE介在性30)・T-細胞介在性19)ともに交差アレルギー反応がみられるため避けるべきである。
このように、現在ではアレルギーは系統だけで判断するのではなく、その化学的構造などを考慮して判断する必要がある。今後、新たなβラクタム系抗菌薬が販売されたとしても、側鎖構造を判断することで交差アレルギーが予測できる。2019年に米国FDAで認可されたcatechol-cephalosporinのCefiderocolは、R1側鎖にセフタジジムと共通の構造を持つ。臨床で使用されないと判定はできないが、セフタジジムやアズトレオナムと交差アレルギーがあるかもしれない。
R2側鎖の類似に関しては、現時点では交差アレルギーとの相関性の研究は不十分であるが、可能であれば避けることが望ましい。しかし、臨床で頻用される抗菌薬ではR2側鎖が類似しているものはない。
複数の系統、側鎖の異なるβラクタム系抗菌薬によって過敏症の既往がある患者では、βラクタム環構造に起因する過敏症の可能性があるため、すべてのβラクタム系抗菌薬が原因となる可能性がある。
【References】
1)Maker JH, Stroup CM, Huang V, et al: Antibiotic Hypersensitivity Mechanisms. Pharmacy (Basel). 2019 Aug 27; 7(3). pii: E122.
2)厚生労働省: 重篤副作用疾患別対応マニュアル「薬剤性過敏症症候群」(平成19年6月改定)
3)厚生労働省: 重篤副作用疾患別対応マニュアル「スティーヴンス・ジョンソン症候群」(平成29年6月改定).
4)厚生労働省: 重篤副作用疾患別対応マニュアル「中毒性表皮壊死融解症(中毒性表皮壊死症)」(平成29年6月改定).
5)厚生労働省: 重篤副作用疾患別対応マニュアル「急性汎発性発疹性膿疱症」(平成21年5月).
6)Mirakian R, Leech SC, Krishna MT, et al; Standards of Care Committee of the British Society for Allergy and Clinical Immunology: Management of allergy to penicillins and other beta-lactams. Clin Exp Allergy. 2015 Feb; 45(2): 300-27.
7)Sullivan TJ, Wedner HJ, Shatz GS, et al: Skin testing to detect penicillin allergy. J Allergy Clin Immunol. 1981 Sep; 68(3): 171-80.
8)Torres MJ, Ariza A, Mayorga C, et al: Clavulanic acid can be the component in amoxicillin-clavulanic acid responsible for immediate hypersensitivity reactions. J Allergy Clin Immunol. 2010 Feb; 125(2): 502-5. e2.
9)厚生労働省: コチニール等を含有する医薬品,医薬部外品及び化粧品への成分表示等について. 薬食審査発0511第1号,薬食安発0511第1号,2012.
10)ワイドシリン®細粒20%添付文書: Meiji Seikaファルマ株式会社, 2018年3月改訂(第4版).
11)Chaudhry SB, Veve MP, Wagner JL: Cephalosporins: A Focus on Side Chains and β-Lactam Cross-Reactivity. Pharmacy (Basel). 2019 Jul 29; 7(3). pii: E103.
12)Uyttebroek AP, Decuyper II, Bridts CH, et al:Cefazolin Hypersensitivity: Toward Optimized Diagnosis. J Allergy Clin Immunol Pract. 2016 Nov-Dec; 4(6): 1232-6.
13)Mota I, Gaspar Â, Morais-Almeida M: Perioperative Anaphylaxis Including Kounis Syndrome due to Selective Cefazolin Allergy. Int Arch Allergy Immunol. 2018; 177(3): 269-73.
14)Blumenthal KG, Peter JG, Trubiano JA, et al: Antibiotic allergy. Lancet. 2019 Jan 12; 393(10167): 183-98.
15)Gaeta F, Valluzzi RL, Alonzi C, et al: Tolerability of aztreonam and carbapenems in patients with IgE-mediated hypersensitivity to penicillins. J Allergy Clin Immunol. 2015 Apr; 135(4): 972-6.
16)Cunha BA, Hamid NS, Krol V, et al: Safety of meropenem in patients reporting penicillin allergy: lack of allergic cross reactions. J Chemother. 2008 Apr; 20(2): 233-7.
17)Wall GC, Nayima VA, Neumeister KM: Assessment of hypersensitivity reactions in patients receiving carbapenem antibiotics who report a history of penicillin allergy. J Chemother. 2014 Jun; 26(3): 150-3.
18)Patriarca G, Schiavino D, Lombardo C, et al: Tolerability of aztreonam in patients with IgE-mediated hypersensitivity to beta-lactams. Int J Immunopathol Pharmacol. 2008 Apr-Jun; 21(2): 375-9.
19)Romano A, Gaeta F, Valluzzi RL, et al: Cross-reactivity and tolerability of aztreonam and cephalosporins in subjects with a T cell-mediated hypersensitivity to penicillins. J Allergy Clin Immunol. 2016 Jul; 138(1): 179-86.
20)Frumin J, Gallagher JC: Allergic cross-sensitivity between penicillin, carbapenem, and monobactam antibiotics: what are the chances? Ann Pharmacother. 2009 Feb; 43(2): 304-15.
21)Pettett BJ, Eskildsen SM, Huang KX, et al: Despite the Safety of Preoperative Cefazolin for Patients With Non-anaphylactic Penicillin Allergy, 20% of Practitioners Avoid Its Use. Orthopedics. 2019 Sep 1; 42(5): e437-42.
22)Macy E, Goldberg B, Poon KY: Use of commercial anti-penicillin IgE fluorometric enzyme immunoassays to diagnose penicillin allergy. Ann Allergy Asthma Immunol. 2010 Aug; 105(2): 136-41.
23)Gugkaeva Z, Crago JS, Yasnogorodsky M: Next step in antibiotic stewardship: Pharmacist-provided penicillin allergy testing. J Clin Pharm Ther. 2017 Aug; 42(4): 509-12.
24)Atanasković-Marković M, Gaeta F, Medjo B, et al: Tolerability of meropenem in children with IgE-mediated hypersensitivity to penicillins. Allergy. 2008 Feb; 63(2): 237-40.
25)Grayson ML, Cosgrove SE, Crowe SM. Lindsay Grayson et al: Kucers’ The Use of Antibiotics: A Clinical Review of Antibacterial, Antifungal, Antiparasitic, and Antiviral Drugs, 7thSeventh eEdition, CRC Press, 2017.
26)Shenoy ES, Macy E, Rowe T, et al: Evaluation and Management of Penicillin Allergy: A Review. JAMA. 2019 Jan 15; 321(2): 188-99.
27)Rubin R: Overdiagnosis of Penicillin Allergy Leads to Costly, Inappropriate Treatment. JAMA. 2018 Nov 13; 320(18): 1846-8.
28)Macy E, Contreras R: Health care use and serious infection prevalence associated with penicillin “allergy” in hospitalized patients: A cohort study. J Allergy Clin Immunol. 2014 Mar; 133(3): 790-6.
29)Turner NA, Moehring R, Sarubbi C, et al: Influence of Reported Penicillin Allergy on Mortality in MSSA Bacteremia. Open Forum Infect Dis. 2018 Feb 19; 5(3): ofy042.
30)Romano A, Valluzzi RL, Caruso C, et al: Cross-Reactivity and Tolerability of Cephalosporins in Patients with IgE-Mediated Hypersensitivity to Penicillins. J Allergy Clin Immunol Pract. 2018 Sep-Oct; 6(5): 1662-72.